Descubren un mecanismo para la formación de plaquetas
El trabajo publicado en la revista Developmental Cell por el grupo de División Celular y Cáncer del Centro Nacional de Investigaciones Oncológicas (CNIO), una institución pública española con sede en Madrid, describe cómo las células originarias de las plaquetas, los megacariocitos, pueden ser reprogramadas de forma artificial a plaquetas y reconstituir sus niveles en sangre
|

Por Ana M. Pertierra
La identificación de esta nueva ruta para generar plaquetas, proceso denominado endociclo y que también se da en otros tipos celulares como ciertas células de la placenta, podría actuar como fuente alternativa de plaquetas cuando los mecanismos habituales fallan. Según los especialistas, los resultados no solo pueden ayudar en el tratamiento de la trombocitopenia, sino también favorecer el diseño de mejores tratamientos terapéuticos en cáncer.
La trombocitopenia es una enfermedad que se caracteriza por un índice inferior al normal de plaquetas, unas células minúsculas que participan en la coagulación de la sangre. Los pacientes suelen sufrir sangrados incontrolados que pueden dar lugar a hematomas y hemorragias, e incluso la muerte. Así, entender cómo se producen estas células en el organismo podría ser de gran utilidad para paliar la enfermedad, cuya incidencia aumenta de manera exponencial en aquellos pacientes sometidos a tratamientos como la quimioterapia. En estos últimos, tal es la gravedad de los síntomas que pueden ser motivo de cese de dicho tratamiento.
FABAINFORMA entrevistó a través del correo electrónico al Dr. Marcos Malumbres, Director del Grupo de División Celular y Cáncer del CNIO, investigador del Consejo Superior de Investigaciones Científicas (CSIC) de España, profesor de la Universidad Autónoma de Madrid y líder del equipo de investigación que llevó a cabo el estudio recientemente publicado en Developmental Cell.

• Dr. Marcos Malumbres, Director del Grupo de División Celular y Cáncer del CNIO
FI- ¿ Cuál fue el objetivo principal del estudio que acaban de publicar en Developmental Cell y cuál su relación con los mecanismos que desencadenan el cáncer?
MM- Nuestro laboratorio está interesado en los mecanismos de división celular y sus diferencias entre células tumorales y normales. Las células tumorales suelen tener dotaciones cromosomales anormales y nos interesaba saber qué distingue a los ciclos celulares que producen células diploides y los que producen poliploidia. Entre las pocas células normales poliploides se encuentran los megacariocitos y decidimos estudiar cómo se regula este ciclo celular tan especial en estas células.
FI - ¿Cuál fue el hallazgo más relevante del estudio y cuáles sus futuros alcances y repercusiones?
MM- Existen básicamente dos mecanismos para formar células poliploides y distintos tipos celulares usan uno u otro. Mediante modificación genética de reguladores de uno otro mecanismo in vivo, nos encontramos que ambos son intercambiables. Esto significa que se pueden formar plaquetas con mecanismos de división celular que usan por ejemplo las células gigantes de la placenta y no los megacariocitos. Además, encontramos que la inhibición de una quinasa del ciclo celular, llamada Cdk1, permite la formación de plaquetas. Estos resultados tienen implicaciones en quimioterapia ya que los inhibidores de Cdks se están considerando ahora para la terapia del cáncer. Dado que la trombocitopenia es un efecto secundario común en estos tratamientos, el generar plaquetas incluso inhibiendo Cdk2 puede resultar en propuestas que impidan estos efectos secundarios en la quimioterapia.
FI- ¿Qué metodología utilizaron y sobre qué modelos animales las aplicaron?
MM- El estudio se realizó mediante modificación genética de ratones, uno de los pocos modelos en mamíferos que permite eliminar uno u otro gen específicamente y ver las consecuencias fisiológicas.
FI- ¿Qué significa que se pueda reprogramar megacariocitos para que generen plaquetas en ciertas condiciones de carencia?
MM- La trombocitopenia, o disminución del número de plaquetas, es una enfermedad que afecta a niños y adultos y en donde la vida puede estar en peligro debido a la imposibilidad de coagulación de la sangre y hemorragias. Hay varios tratamientos basados en rutas indirectas. Nuestros datos abren la posibilidad de que algunos pacientes, en los que la trombocitopenia se deba a problemas con el ciclo celular normal de los megacariocitos, puedan producir plaquetas basadas en la nueva vía descrita en nuestro trabajo.
FI- ¿Considera que este conocimiento aportado por su grupo de investigación puede ser de utilidad para tratamientos más eficaces contra el cáncer?
MM- La trombocitopenia es uno de los efectos secundarios indeseables más frecuentes en los tratamientos actuales de quimioterapia. En algunos casos, por ejemplo en las terapias dirigidas contra la división celular o mitosis, los fármacos que inhiben quinasas mitóticas impiden la endomitosis propia de los megacariocitos. Nuestros datos indican que se pueden diseñar tratamientos alternativos, por ejemplo inhibiendo Cdk1, en los que podamos prevenir la mitosis de las células tumorales pero en los que los megacariocitos no se verán afectados ya que pueden generar plaquetas mediante la nueva vía descrita. Sin embargo, es importante señalar que nuestros datos se han realizado en modelos celulares y animales y la aplicación directa requerirá muchos más estudios.
FI- ¿Qué otros estudios serán necesarios para su traslación a la farmacología clínica?
MM- La posibilidad de generar plaquetas en ausencia de la ruta normal que los megacariocitos usan abre ciertas posibilidades todavía por explorar. Por ejemplo sería interesante comparar la formación de plaquetas por células madre usando la vía normal o la alternativa y ver en qué condiciones se generar más y mejores plaquetas, o cual de esas condiciones es mejor para generar plaquetas en pacientes con enfermedades específicas. Para trasladar estas ideas a la clínica son necesarios estudios adicionales en modelos con trombocitopenias específicas (ya que su causa genética o fisiológica es muy variada de paciente a paciente). Además, todavía no hemos realizado estudios en células humanas e idealmente se deberían probar células madre o progenitoras humanas, si es posible obtenidas de pacientes con trombocitopenia, y usar sobre ellas inhibidores específicos de distintos reguladores de las vías alternativas y ver su efecto en la generación de plaquetas.
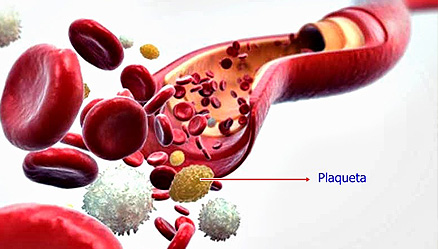
Megacariocitos: células gigantes
Las plaquetas se producen de una forma muy peculiar y poco frecuente en humanos, incluso en otras células animales: los megacariocitos crecen durante su desarrollo hasta que se convierten en células gigantes para posteriormente 'romperse' y formar las células diminutas que son las plaquetas. Este impulso de crecimiento ocurre a través de varias rondas de duplicación de material genético, que resultan en células de gran tamaño con un número de juegos completos de cromosomas mayor al habitual.
Los megacariocitos son células gigantescas de la médula ósea que mediante fragmentación de su citoplasma dan origen a las plaquetas. Por lo tanto, las plaquetas son fragmentos de megacariocitos que circulan por la sangre y desempeñan funciones importantes en su coagulación, evitando que una persona se desangre al sufrir una herida.
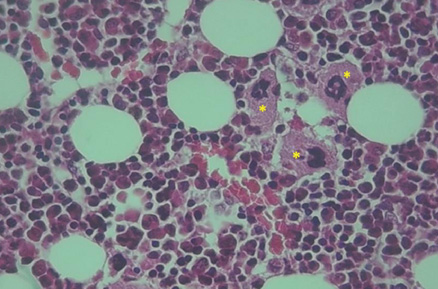
• Médula ósea panorámica 400 X. Los megacariocitos se señalan con los asteriscos amarillos
También participan en la reparación de los tejidos lesionados produciendo sustancias que promueven la cicatrización.
Los megacariocitos miden entre 30 y 100 micrómetros de diámetro; son de núcleo polilobulado y poliploide, es decir, contienen una cantidad mayor de ADN que las células normales diploides.
Se originan en las Unidades Multipotenciales No Linfoides (UMNL) de la médula ósea. Las UMNL dan origen, mediante mitosis y diferenciación, a varias células progenitoras de líneas hemocitopoyéticas no linfoides, las llamadas Unidades Formadoras de Colonias (UFC), las cuales son: UFC Granulocito – Macrófago, UFC Megacariocítica, UFC Eritroide, UFC de Basófilos, UFC de Eosinófilos.
Las Unidades Formadoras de Colonias Megacariocíticas (UFCM) no son fáciles de identificar mediante el examen corriente de la biopsia o del aspirado (mielograma) de la médula ósea; miden alrededor de 15 micrómetros de diámetro y son similares a un linfocito grande. Estas UFCM mediante mitosis y diferenciación dan origen a los promegacarioblastos pueden identificarse con la coloración de Inmunohistoquímica.
Los Promegacarioblastos se diferencian y mediante mitosis, sólo del núcleo, sin división del citoplasma (fenómeno llamado endomitosis sin citocinesis), dan origen a los Megacarioblastos, células gigantes de entre 30 y 50 micrómetros de diámetro, cuyo núcleo ya es lobulado y pueden identificarse con microscopia de luz y coloraciones de Wright.
Los megacarioblastos mediante endomitosis incompleta, sin citocinesis, dan origen a los megacariocitos, células poliplodes (hasta más de 16N) los cuales por fragmentación citoplasmática dan origen entre 4.000 y algo más de 6.000 plaquetas.
La posibilidad de generar plaquetas en ausencia de la ruta normal que los megacariocitos usan abre ciertas posibilidades todavía por explorar. Por ejemplo sería interesante comparar la formación de plaquetas por células madre usando la vía normal o la alternativa y ver en qué condiciones se generar más y mejores plaquetas, o cual de esas condiciones es mejor para generar plaquetas en pacientes con enfermedades específicas
|
|
|






