Epigenética, el futuro
para la reprogramación celular
Un equipo de investigación argentino ha logrado poner en práctica un concepto novedoso en el manejo de las células madre. Se trata de la reprogramación directa que consiste en modificar las marcas epigenéticas de un gen en una célula adulta para transformarla en otra. Así consiguieron obtener células productoras de insulina a partir de células de la piel de pacientes diabéticos.
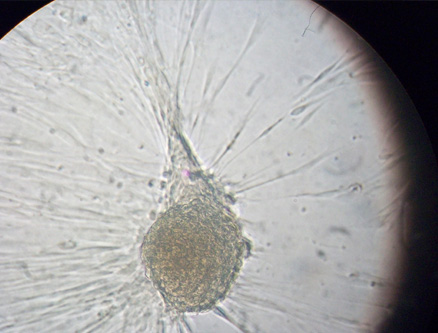
• Agrupación celular que produce insulina formada a partir de fibroblastos transformados químicamente de pacientes con diabetes tipo I.
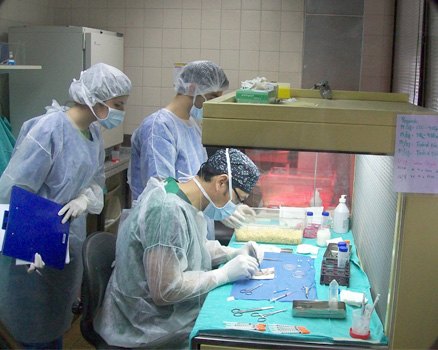
• Parte del equipo realizando los trasplantes de las células productoras de insulina en ratones diabéticos (de izq a der: Lic Carla Giménez, Lic Nelson Rueda, Cirujano Dr Sung-Ho Hyon)
Por Ana M. Pertierra
El proyecto de investigación aplicada llevado a cabo por un grupo de 12 científicos a cargo del doctor Federico Pereyra Bonnet y dirigidos por el Dr. Pablo Argibay en el Instituto de Ciencias Básicas y Medicina Experimental del Hospital Italiano de la ciudad de Buenos Aires, les valió un amplio reconocimiento a nivel internacional y la obtención del premio Innovar 2012 otorgado por el Ministerio de Ciencia y Tecnología, a nivel nacional. El procedimiento constituye un innovador método, en el que sin mediar transgénesis, consiguen transformar células epiteliales en células productoras de insulina.
En el campo de la investigación con células madre existen tres tipos de ellas: las embrionarias, que generan todas las células adultas del organismo, las adultas, que pertenecen a distintos tejidos y que permanentemente están renovando el stock celular del organismo y las reprogramadas o células madre pluripotentes inducidas (normalmente abreviadas como células iPS, por sus siglas en inglés: “induced Pluripotent Stem” ), un descubrimiento de laboratorio que le valió el Nobel de Medicina 2012 a Shinya Yamanaka mediante el cual a partir de células adultas (fibroblastos) logró, mediante la transferencia de cierto material genético vehiculizado por virus, volverlas a un estado de célula embrionaria con capacidad para generar cualquier tipo de células.
Ahora los científicos plantean un método innovador a nivel mundial porque realiza la reprogramación de células obtenidas a partir de la piel, los fibroblastos, de pacientes con diabetes tipo 1 para convertirlas en células que expresan genes pancreáticos (insulina, glucagon y somatostatina). Y para lograrlo no modifican genéticamente a las células tratadas ni utilizan células madre embrionarias, sino que lo hacen mediante la aplicación de sustancias químicas.
En diálogo con FABAINFORMA, el doctor Federico Pereyra Bonnet describió el fenómeno de plasticidad celular que les permite encarar los estudios de terapias celulares. “Los genes que están dentro de toda célula pueden prenderse y apagarse. El cigoto es una célula con un único núcleo y a partir de ella se generan 200 tipos de células distintas que tienen el mismo ADN. ¿Por qué una célula es una neurona y otra una célula beta? Porque ciertos genes están prendidos y otros apagados, pero eso no significa que estén silenciado de por vida, este descubrimiento le valió el Nobel a Yamanaka”, explicó Pereyra Bonnet.

• El investigador Dr Pereyra-Bonnet Federico (der) junto con el Dr Argibay (izq) director del proyecto
“Para mí, toda célula adulta puede llegar a ser célula madre”, dijo. Sin embargo –agrega el científico– lo difícil es direccionar a una célula madre hacia la diferenciación que uno quiere”.
Epigenética en la reprogramación directa
Para que un gen se exprese requiere de un promotor, una secuencia específica de ADN localizada justo donde se encuentra el punto de inicio de la transcripción del ADN que contiene la información necesaria para activar o desactivar el gen que regula.
“Si el promotor de un gen está metilado (unido a un sencillo grupo -CH3) en sitios específicos, la maquinaria de transcripción no se puede acoplar, el gen no se puede transcribir y por lo tanto está apagado. También ocurren metilaciones en otros sitios como en las histonas y además se producenen ubiquitinazaciones y fosforilaciones que regulan la expresión de los genes, y a todo esto se lo llama epigenética, que significa `arriba de los genes´”, explicó Pereyra Bonnet.
Las investigaciones en el campo de la epigenética abren un amplio horizonte para las terapias celulares.
“Si se logran sacar los grupos metilo a un gen específico que se encuentra apagado, el gen se puede expresar y eso se llama reprogramación directa, un camino más corto que no requiere llevar al fibroblasto al estadio de pluripotencialidad, para luego diferenciarlo en célula pancreática (propuesto por Yamanaka)”, sostuvo Pereyra Bonnet, quien reconoció que “no es una tarea fácil pero ofrece ciertas ventajas respecto a las IPS, que in vitro son excelentes y han resuelto muchos problemas, pero que conllevan el riesgo de que se disparen tumores”. Según Pereyra Bonnet, cuando se llega al estadio de células madre con todos los genes prendidos existe el riesgo de despertar genes potencialmente problemáticos como los generadores de tumores y además es grande el estrés que se le provoca a la célula con una remodelación total”.

• Frascos de cultivo celular donde se hace la transformación química de los fibroblastos de pacientes con diabetes tipo I.
El investigador describió el trabajo desarrollado en el Instituto de Ciencias Básicas y Medicina Experimental del Hospital Italiano que consiste en obtener células de la piel, fibroblastos, de pacientes diabético tipo 1 a partir de una biopsia y someterlos al tratamiento con diferentes sustancias químicas que son capaces de “despertar” el gen productor de insulina.
“Lo que obtenemos in vitro no es una célula beta (pancreática) perfecta sino una célula parecida, un fibroblasto que expresa las principales hormonas de la célula beta (insulina, glucagon, somatostatina)”, explicó Pereyra Bonnet y –añade–“el tratamiento químico que transforma la célula de la piel en célula tipo pancreática tiene una alta eficiencia cercana al 30%. El fibroblasto tiene una epigenética que lo hace un buen candidato para transformarlo en célula beta pancreática porque cuando lo analizamos mediante técnicas de PCR bisulfito e inmunoprecipitación de cromatina vemos que está débilmente metilado”.
Las sustancias químicas utilizadas para el tratamiento de reprogramación celular son las mismas que aparecen durante la génesis pancreática. “Son unas 20 moléculas que se producen durante los distintos estadios del desarrollo pancreático y que se van incorporando en los cultivos celulares de forma secuencial, entre ellas complejos proteicos como la activina, factores de crecimiento, vitaminas como la nicotinamida y exedin 4, una droga que se da como tratamiento a los diabéticos, entre otras”, detalla el investigador.
De las pruebas realizadas con ratones, trasplantes intrapancreáticos de las células transdiferenciadas productoras de insulina, han obtenido resultados sumamente alentadores. “En los ratones diabéticos trasplantados encontramos que había insulina humana circulante, y aunque la diabetes no revirtió, protegió a los ratones de la pérdida de peso y mejoró los síntomas de la enfermedad. Eso quiere decir que todavía nos falta para llegar a células más maduras”.
El futuro de una terapia celular para diabéticos
La diabetes tipo 1 es una enfermedad crónica que afecta sólo a un tipo de células, las beta pancreáticas. Es una enfermedad autoinmune que provoca la autodestrucción de las células productoras de insulina. La glucemia en estos pacientes debe manejarse mediante inyecciones de insulina, sin embargo, no es posible el control preciso de los valores de glucosa en sangre y los pacientes sufren de complicaciones asociadas de tipo renales, oculares y circulatorias. Según señala Pereyra Bonnet, el Hospital Italiano hace casi tres décadas que está dedicado al estudio de tratamientos alternativos para la diabetes. El doctor Pablo Argibay, médico cirujano, director del ICBYME y del proyecto de investigación sobre reprogramación celular ha sido un pionero en trasplante de páncreas entero para casos extremos de pacientes tipo 1, y de islotes de células beta de donante cadavérico. Sin embargo, estos tratamientos tienen ciertas limitaciones tales como el rechazo y la falta de donantes. En los últimos diez años y con el advenimiento de las nuevas tecnologías, el foco de las investigaciones está puesto en las terapias celulares. Los estudios de reprogramación celular que los científicos del ICBYME del Hospital Italiano están desarrollando con muestras de piel de cuatro pacientes de diabetes tipo 1, bajo las condiciones de consentimiento informado, y de protocolos aprobados por los correspondientes comités de ética, aspiran a alcanzar un tratamiento celular eficaz para los próximos años.
|
|