Descubren un posible tratamiento para la cirrosis
Investigadores españoles han demostrado en modelos experimentales que interfiriendo a la proteína CPEB4, una molécula mediadora en el proceso de angiogénesis, se podría evitar la generación de nuevos vasos sanguíneos anómalos asociados a la cirrosis. Este hallazgo, que se publica en la revista Gastroenterology, abre las puertas al desarrollo de un inhibidor con potencial terapéutico para la aplicación clínica
Por Ana M. Pertierra
La cirrosis es una lesión crónica del hígado caracterizada por la acumulación de cicatrices (nódulos fibrosos) en el tejido que interfieren en la estructura y el funcionamiento normal del órgano. Las principales causas de las lesiones hepáticas crónicas son la infección por hepatitis B o C y el alcoholismo, las menos comunes incluyen: Hepatitis autoinmunitaria, trastornos en las vías biliares, algunos medicamentos, enfermedades hereditarias y otras enfermedades hepáticas como esteatosis hepática no alcohólica (NAFLD, por sus siglas en inglés) y esteatohepatitis no alcohólica (NASH, por sus siglas en inglés). La cirrosis es el mayor factor de riesgo para la aparición de cáncer de hígado.
En los países occidentales, la cirrosis hepática se encuentra entre las primeras 10 causas de muerte en adultos y entre las primeras de trasplante hepático.
El cúmulo de cicatrices complica la circulación de la sangre a través del hígado, generando hipertensión portal (de la vena porta). Para liberar presión en la vena, se generan vasos sanguíneos colaterales, fuera del hígado. El problema entonces es doble, primero porque todavía llega menos sangre al hígado lo que genera más daño hepático y además los vasos son de mala calidad (angiogénesis patológica).
Un grupo de científicos liderados por Raúl Méndez, investigador ICREA del Instituto de Investigación Biomédica (IRB Barcelona), y Mercedes Fernández, del IDIBAPS de Barcelona, identificaron un mecanismo de sobreexpresión del factor angiogénico que promueve una angiogénesis patológica regulada por acciones secuenciales de las proteínas CPEB1 y CPEB4. Por ello, los científicos señalan a la proteína CPEB4 como la molécula a inhabilitar para evitar la generación de nuevos vasos sanguíneos anómalos asociados a cirrosis.
La angiogénesis patológica es una de las complicaciones más importantes en pacientes con cirrosis y un factor clave en el desarrollo y agravamiento de la enfermedad. Por ello, se investigan terapias para combatirla. Los resultados del estudio se acaban de publicar en el último número de la revista científica Gastroenterology (Gastroenterology (2015). doi: 10.1053/j.gastro.2015.11.038)
Los especialistas explican que "cuando las células hepáticas intentan reparar las lesiones el modo en que lo hacen acaba siendo fatal para el órgano. Un círculo que se va amplificando y que acaba siendo muy crítico para la vida de los pacientes. Además, los vasos colaterales forman varices en el esófago y estómago de los pacientes con cirrosis; estas varices son muy frágiles y son propensas a romperse causando hemorragias intensas y muy difíciles de parar", explica Mercedes Fernández, del IDIBAPS y co-líder del estudio. "Por ello, una terapia dirigida a revertir los vasos patológicos, que no existe hoy por hoy, sería eficiente", añade.
Según los investigadores, este circuito reparador en el que entra el hígado empeora tanto la situación que provoca que los nódulos de regeneración, con altos niveles de CPEB4, acaben formando hepatocarcinomas. Actualmente, los fármacos buscan evitar la neovascularización mediante la inhibición de VEGF o los receptores de VEGF, pero sus efectos adversos no son tolerables porque de forma indiscriminada inhiben la generación normal de los vasos. De allí, el interés de la comunidad científica en la búsqueda de otras dianas alternativas.
La angiogénesis se convierte en un proceso patológico
FABAINFORMA se comunicó a través del correo electrónico con Mercedes Fernández, Doctora en Biología por la Universidad de Barcelona, Jefe de Grupo en el Instituto de Investigaciones Biomédicas IDIBAPS y en el CIBERehd y autora del trabajo que se acaba de publicar en Gastroenterology.

• Mercedes Fernández, Doctora en Biología por la Universidad de Barcelona, Jefe de Grupo en el Instituto de Investigaciones Biomédicas IDIBAPS y en el CIBERehd y autora del trabajo que se acaba de publicar en Gastroenterology.
-¿Cuál ha sido el mayor aporte al conocimiento del mecanismo responsable del agravamiento de la enfermedad hepática crónica que se desprende de las conclusiones del trabajo que su equipo acaba de publicar en Gastroenterology?
La angiogénesis patológica y la sobreexpresión del factor de crecimiento endotelial vascular, VEGF, (por sus siglas del inglés), que caracterizan a la enfermedad hepática crónica están promovidas de forma específica por unas proteínas llamadas CPEB (cytoplasmic polyadenylation element - binding proteins). Lo más bonito del trabajo es que demostramos que interfiriendo con las proteínas CPEB4 eliminamos únicamente la formación de vasos patológicos, mientras que la vascularización positiva se mantiene intacta.
-¿Qué función se le ha demostrado a las proteínas CPEB y por qué se augura que podrían ser una futura diana terapéutica para la cirrosis?
Las proteínas CPEB1 y CPEB4 regulan de forma secuencial la expresión patológica y excesiva de VEGF asociada a la enfermedad hepática crónica, pero no la expresión basal de VEGF, la cual es necesaria para que los vasos sanguíneos sanos funcionen con normalidad.
¿Esta relación entre CPEB4 y angiogénesis, a través de VEGF, puede también explicarse en el desarrollo de tumores?
En un estudio anterior publicado en Nature Medicine, el grupo de Raúl Méndez descubrió que la CPEB4 interviene en la formación de vasos sanguíneos en cáncer de páncreas y cerebro. Actualmente, estamos trabajando de forma coordinada con Raúl Méndez y con Jordi Bruix para desentrañar el papel de esta molécula en carcinoma hepatocelular, el principal cáncer de hígado.
¿En qué condiciones la angiogénesis se transforma en un mecanismo patológico?
En una enfermedad, hay cambios en el equilibrio local de diversos factores reguladores que hacen que la angiogénesis se convierta en un proceso patológico, con la formación excesiva de nuevos vasos sanguíneos anómalos. Esta angiogénesis acompaña y favorece la progresión y el agravamiento de la enfermedad, como sucede en la enfermedad hepática crónica.
-Este trabajo experimental es de la ciencia básica. ¿Cuántos otros estudios y reglamentaciones se requieren para llegar a una aplicación clínica?
En primer lugar, hay que desarrollar un inhibidor de las proteínas CPEB que tenga potencial terapéutico en la clínica, que pueda ser aplicado al humano. Estamos actualmente trabajando en ello. Una vez identificado, tendremos que validarlo en diferentes estudios en modelos animales y modelos in vitro antes de poder aplicarlo a la clínica.
-¿Con qué modelos animales trabajaron en este estudio?
Utilizamos animales modificados genéticamente (ratones knockout), los cuales carecían de las proteínas CPEB4 o CPEB1. También usamos modelos de cirrosis e hipertensión portal.
- ¿Qué repercusión ha tenido esta investigación en la comunidad científica?
Está teniendo una elevada repercusión tanto en la comunidad científica como en la sociedad en general gracias a la divulgación de la noticia a través de la prensa.
- ¿Qué futuros estudios en este tema tienen programados en la Universidad de Barcelona?
Estudiar la función de las proteínas CPEB en el desarrollo del cáncer de hígado y desarrollar inhibidores de estas proteínas con potencial terapéutico en la clínica.
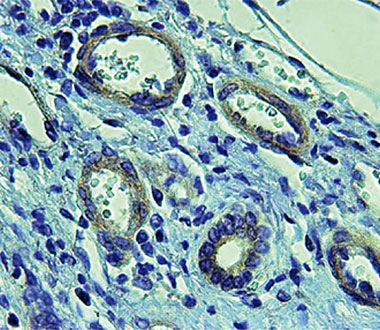
Vasos patológicos (círculos blancos), con abundante expresión de la proteína CPEB4, en tejido cirrótico. / IRB BARCELONA/IDIBAPS
|
|
|