Enfermedades antiguas de reciente aparición comprobada en la Argentina
El Comité de Redacción de Acta Bioquímica Clínica Latinoamericana ha seleccionado este artículo publicado en CIENCIA HOY - Volumen 19 Número 114 (diciembre 2009 – enero 2010), para su difusión a través de FABA Informa.
Las leishmaniasis se conocen como enfermedades humanas desde hace siglos, pero en las últimas décadas se han transformado en un serio problema de salud pública en los noventa países en que son actualmente endémicas. Se estima que hoy contraen leishmaniasis cutánea 1,5 millones de personas por año, y 500.000 adquieren leishmaniasis visceral. Unas 350 millones de personas están en situación de riesgo de enfermar.
Conceptos básicos
Patricio Garrahan
Instituto de Química y Fisicoquímica Biológicas, UBA-Conicet
Las leishmaniasis son enfermedades provocadas por parásitos protozoarios del género Leishmania, es decir, por organismos unicelulares que, a diferencia de las bacterias, poseen núcleos y mitocondrias, como los seres multicelulares.
El parásito se transmite entre los diversos seres vivientes a los que infecta mediante la picadura de la hembra de un insecto volador cuyo tamaño es aproximadamente un tercio del de un mosquito. En la Argentina suele llamárselo torito, carachai o jején; en inglés su nombre coloquial es sand fly, esto es, mosca de la arena. No genera en vuelo el típico zumbido de los mosquitos y su picadura puede ser molesta pero no deja roncha persistente.
Las leishmaniasis se presentan en tres formas: cutánea, mucosa y visceral. La leishmaniasis cutánea provoca úlceras en la piel, que aparecen luego de un tiempo en el lugar donde picó el insecto y suelen tener un borde rojizo elevado y una depresión central. Se cubren por una costra y si no se infectan no son dolorosas; pueden cicatrizar espontáneamente en un proceso muy lento que dura meses o años y deja cicatrices deformantes. En algunos pacientes se produce en la región de las úlceras una inflamación de ganglios linfáticos.
Las lesiones cutáneas se pueden extender a las mucosas nasal y bucal, por lo que también se habla de leishmaniasis mucosa, que puede aparecer mucho después de la curación de la forma cutánea.
La leishmaniasis visceral es mucho más grave porque invade órganos internos, en particular el hígado, el bazo y la médula ósea. Los enfermos suelen padecer fiebre, pérdida de peso y un aumento del tamaño del bazo y del hígado, así como una disminución del contenido sanguíneo de glóbulos rojos y plaquetas. Se está convirtiendo en una importante infección oportunista en pacientes cuya inmunidad está deprimida por el sida.
Cada año se producen en el mundo alrededor de un millón y medio de casos de leishmaniasis cutánea y medio millón de la forma visceral, la mayor parte en zonas tropicales y subtropicales. No existe de manera endémica en Australia, Chile, Uruguay y la mayor parte de la Argentina, pero desde 1985 se registran epidemias de la forma cutánea en el norte de este último país, y a partir de 2006 se vienen comprobando en cuatro provincias casos de la forma visceral de la enfermedad.
No se dispone de vacunas u otras formas de prevenir la leishmaniasis, salvo las medidas habituales para evitar picaduras de los insectos que la transmiten, por lo que conocer los sitios, las épocas y las horas de actividad de estos es de suma importancia para evitar la enfermedad. Debe sospecharse su presencia en personas que, habiendo residido en regiones donde es endémica, presenten signos que la sugieran.
El parásito se identifica en muestras sospechosas examinándolas mediante microscopio teñidas con un colorante llamado Giemsa. También es útil aislar y cultivar el parásito, así como analizar su desarrollo en animales de experimentación. La detección de anticuerpos es valiosa en las formas viscerales, pero tiene importancia reducida en las formas cutáneas. Suele haber reactividad cruzada entre los anticuerpos inducidos por Leishmania y los correspondientes al Trypanosoma cruzi, el causante de la enfermedad de Chagas.
Las leishmaniasis en detalle
Oscar Daniel Salomón
Centro Nacional de Diagnóstico e Investigación de Endemo-Epidemias
Mal de muchos
Narradas en tabletas de arcilla del palacio de Nínive, reproducidas en huacos precolombinos y atribuidas a la picadura de un insecto por Avicena alrededor del año 1000 de nuestra era, las leishmaniasis fueron asociadas con los protozoarios que las provocan a fines del siglo XIX. Su nombre fue puesto en honor de William Boog Leishman (1865-1926), un patólogo y médico militar escocés que en 1903 describió esos parásitos unicelulares al observarlos con un microscopio en los órganos de un soldado muerto en Londres que había enfermado tres años antes en Calcuta de una fiebre allí llamada dum-dum o kala-azar.
Hoy, con los métodos de la biología molecular, se ha identificado una treintena de especies de leishmania que infectan a mamíferos, de las que veintiuno provocan enfermedades humanas. Las leishmaniasis se concentran en regiones tropicales, pero se extienden a zonas templadas, como las costas de la cuenca del Mediterráneo; en América se las encuentra desde Texas hasta el centro de la Argentina. La transmisión del parásito a humanos se ha comprobado en unos noventa países de América, África, Asia y Europa, pero no en Oceanía, donde, sin embargo, se han aislado parásitos en canguros.
Las especies de leishmania tienen en común que, una vez ingresado el protozoario en el cuerpo de un mamífero, es capturado por las células de su sistema de defensa y en ellas se reproduce. Diferentes especies no tienen preferencia por los mismos órganos y provocan distintas enfermedades, como leishmaniasis cutánea, leishmaniasis mucosa y leishmaniasis visceral.
Gran parte de los síntomas asociados con estas enfermedades no son el resultado de una acción directa del parásito, sino una reacción del organismo infectado ante su presencia. Por ello, las manifestaciones clínicas dependen tanto de la especie de leishmania como de la respuesta del individuo.
Otro elemento común a este grupo de parásitos es que todos son transmitidos por insectos vectores de la subfamilia Phlebotominae, por la común llamados flebótomos en
la literatura técnica, aunque cada especie de leishmania es transmitida por una o pocas especies de esos insectos. Esa asociación única se produce por un reconocimiento mutuo de moléculas específicas de la cubierta del parásito y del intestino del vector. Por ello, el primero logra multiplicarse y anclarse en el insecto sin ser arrastrado en el proceso de digestión de este.
Los insectos adultos miden entre dos y tres milímetros de largo y tienen alas erectas en forma de V. Se alimentan de azúcares vegetales, pero la hembra, además, ingiere sangre para producir huevos. Suelen estar activos entre el crepúsculo y el amanecer. Las larvas se crían en tierra húmeda con abundante material orgánico en descomposición.
En América los flebótomos se encuentran en ambientes boscosos, mientras en el Viejo Mundo aparecen también en desiertos, lo que explica su nombre inglés de moscas de arena. Un mismo nombre común puede corresponder a distintos insectos y un mismo insecto puede ser conocido por varios nombres comunes, como ocurre en países de habla castellana, donde para los flebótomos se usan, por lo menos, las denominaciones de jejenes, palomillas, toritos y carachais. Sin embargo, por jején se suele designar a otra familia de insectos, los simúlidos (Simuliidae), que no transmiten leishmaniasis. En
Italia el término difundido es pappataci, palabra que ha dado origen al nombre científico de una especie frecuente, Phlebotomus papatasi, y posiblemente al apodo papparazzo (plural papparazzi) del personaje de Federico Fellini en La dolce vita, molesto como un flebótomo. Es que estos insectos pueden resultar abrumadores, a pesar de su pequeño tamaño, por sus ataques en bandada y sus picaduras dolorosas, aunque estas apenas dejan manchas rosadas, sin punto de sangre, que desaparecen al poco tiempo.
Algunas especies de mamíferos se infectan y se convierten en una fuente eficaz de parásitos para los insectos transmisores o vectores. Son, así, reservorios, presenten o
no síntomas. Otros mamíferos infectados actúan como hospedadores (más frecuentemente llamados huéspedes) accidentales de Leishmania y, aunque contraigan la enfermedad y sean picados por los flebótomos vectores, no son fuente de su propagación.
El ser humano pertenece a esta categoría de huésped accidental. Se infecta a partir de la picadura de un flebótomo que ha picado antes a un animal infectado. Por ello se califican las leishmaniasis de zoonosis o enfermedades transmitidas entre animales y humanos. La búsqueda del reservorio y de un animal que permitiese reproducir el parásito en laboratorio condujo a la cría en 1930 de un roedor silvestre de Siria, donde las leishmaniasis cutáneas son endémicas desde hace siglos, animal experimental distribuido luego a todo el mundo como hámster sirio o dorado (Mesocricetus auratus) .
Las distintas leishmaniasis tienen diferentes vectores, reservorios, ecología, epidemiología y consecuencias en salud pública, según la especie del parásito y la región geográfica. Las formas clínicas de las leishmaniasis humanas más frecuentes son:
• Leishmaniasis cutánea: produce una o varias úlceras en la piel. Su curación espontánea, sin tratamiento, es muy lenta y llega a durar años. Dejan cicatrices muy visibles que pueden provocar discriminación social.
• Leishmaniasis mucosa: destruye progresivamente las mucosas y los cartílagos nasales y bucales; provoca mutilaciones, discapacidad y complicaciones graves. Se genera usualmente por falta de tratamiento o tratamiento incompleto de leishmaniasis cutáneas producidas por algunas especies de Leishmania. Los reservorios de los parásitos que provocan leishmaniasis cutáneas y mucosas son mamíferos silvestres.
• Leishmaniasis visceral o kala-azar: se manifiesta por fiebre, pérdida de peso y aumento del tamaño del bazo y del hígado, órganos donde se concentran los parásitos, igual que en la médula ósea. En la India y el Sudán, el reservorio es humano; en Iberoamérica, lo es principalmente el perro, mientras los humanos son huéspedes accidentales, con una letalidad del 6 al 10%, que supera el 90% sin tratamiento.
En las últimas décadas las leishmaniasis están aumentando en cantidad de casos por año y en dispersión geográfica. Se estima que se producen por año en el mundo hasta 1,5 millones de casos nuevos de leishmaniasis cutánea y 500.000 de leishmaniasis visceral; habría doce millones de personas enfermas, y 350 millones expuestas. Sólo en una epidemia de leishmaniasis visceral del este de la India se habrían enfermado en 1996 unas 250.000 personas, mientras que en la que comenzó en 1984 en la provincia del Alto Nilo Occidental, en el Sudán, habrían muerto 100.000 de los 300.000 individuos en riesgo. En Kabul, capital de Afganistán, en 2002 enfermaron de leishmaniasis cutánea 270.000 personas. Por ello, la Asamblea Mundial de la Salud de 2007 priorizó las acciones de control de la leishmaniasis. Entre las herramientas actuales de control están el diagnóstico temprano, el tratamiento oportuno con ciertas drogas (antimoniales pentavalentes, anfotericina, miltefosina), la disminución del contacto con el vector para evitar su picadura y la eliminación del reservorio en el caso de la leishmaniasis visceral americana.
Aunque el cambio climático global puede haber ampliado la distribución de las leishmaniasis, su persistencia estacional o su intensidad, existen otras amenazas más inmediatas que han producido su dramático aumento en los últimos años. Son la deforestación y la adaptación de vectores selváticos en el ambiente modificado; las migraciones humanas y la urbanización desordenada, que aumentan la vulnerabilidad social y ambiental; el incremento del número de individuos con sus sistemas inmunitarios comprometidos, por ejemplo, por el sida o por la desnutrición, y el suministro a mascotas de drogas para tratamiento humano, lo que favorece la selección de los parásitos más virulentos. La Argentina no ha sido ajena a este incremento de casos de leishmaniasis cutánea, ni a la expansión de la leishmaniasis visceral.
Leishmaniasis cutáneas en la Argentina:
una resurrección provocada
Estas leishmaniasis han sido formalmente registradas en la Argentina desde la segunda década del siglo XX, gracias al trabajo de precursores como William Paterson
(1871-1946) y Salvador Mazza (1886-1946), aunque su presencia anterior en la región viene sugerida por vocablos quechuas como uta y espundia. En 1925 viajó al noroeste argentino el bacteriólogo francés Charles Nicolle (1866-1936), que recibió el premio Nobel de medicina en 1928 por su descubrimiento de la forma de transmisión del tifus. Había sido invitado por Mazza, quien lo conoció en ocasión de una estadía en el Instituto Pasteur de Túnez. Nicolle y Mazza, junto con Ricardo Alvarado, director del
Consejo de Higiene de Jujuy, aislaron los parásitos de la leishmaniasis americana en un medio de cultivo que aún hoy se utiliza y lleva el nombre del investigador francés. Hacia 1930 se realizó el primer censo de pacientes de la enfermedad, la mayoría de los cuales fueron hombres en edad laboral, que trabajaban en selvas y bosques del norte.
Luego se produjo una disminución de nuevos casos, al ritmo de la desaparición de la vegetación original, lo que llevó a predecir la desaparición de la enfermedad junto con la de los ecosistemas que la sustentaban. Sin embargo, tanto en el Brasil como en la Argentina, emergió en la década de 1980 en forma de epidemia.
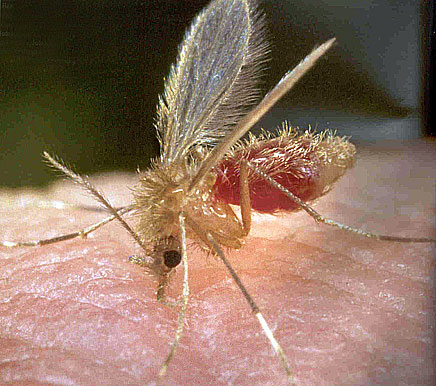
> Flebótomo de la especie phlebotomus papatasi en el momento de succionar sangre humana, que se advierte en su abdomen. Imagen Centres for Disease Control, Wikipedia Commons. Foto James Gathany.
La primera epidemia registrada en la Argentina comenzó en 1985 en el noroeste de la provincia de Salta. Se produjeron luego brotes en otras provincias norteñas. en áreas ubicadas al pie de la selva húmeda subtropical de yungas, que luego se extendieron a la región del monte chaqueño y, finalmente, llegaron a la selva subtropical paranaense. Hoy la enfermedad ha vuelto a estar presente en toda su área histórica, que abarca unos 500.000 km2 y comprende sectores de las provincias de Salta, ]ujuy, Tucumán, Catamarca, Santiago del Estero, Formosa, Chaco, Corrientes y Misiones. Entre 1984 y 2008 el sistema de salud registró 7947 casos en la Argentina. con una mayor proporción de mujeres y niños que en 1930. Debido al diagnóstico temprano y al acceso a tratamiento estándar, se redujo la proporción de enfermos de leishmaniasis cutánea que desarrollan con los años una leishmaniasis mucosa.
El parásito aislado con mayor frecuencia durante estas epidemias pertenece a la especie Leishmania braziliensis. De las veinticinco especies de flebótomos encontradas en la Argentina, una (Lutzomyia neivai) ha sido incriminada como el principal vector del parásito por estar presente en gran abundancia durante los brotes epidémicos, picar a humanos y a animales, y haberse encontrado que estaba infectada por Leishmania braziliensis. Ningún animal cumplió hasta el momento los requisitos para ser considerado su reservorio, aunque humanos, equinos, caninos y felinos pueden ser huéspedes accidentales.
Lutzomyia neivai se cría en parches de vegetactón cerrada y en selvas en galería en las costas de ríos, desde donde puede colonizar periódicamente ambientes modificados, como patios de las viviendas, aunque no pueda mantener en estos una poblacíón permanente. Su abundancia tiene dos o tres picos anuales, regulados por la temperatura y la lluvia. Estas dos características, que generan aumentos explosivos de vectores en un sitio y un momento determinados, si coinciden con actividades humanas que incrementan la exposición a ellos, provocan la aparición de epidemias.
Así, los deforestadores pueden contraer leishmaniasis cutánea por trabajar en el ambiente que habitan los vectores y reservorios silvestres, pero también puede enfermarse la población que se instala con animales domésticos inmediatamente después de la deforestación, o en casas próximas al borde del monte. Esto ocurrió cuando se trasladó el pueblo de Vinalito en Jujuy, y en los alrededores de Puerto Iguazú, con la ocupación humana de áreas selváticas.
La modificación del ambiente también puede originar una epidemia por el desplazamiento excepcional y temporario de los vectores. En el río Bermejo, un desborde concentró al flebótomo Lutzomyia neivai en un sitio visitado por pescadores, lo que resultó en un brote de leishmaniasis cutánea en Las Lomitas, Formosa. La deforestación contigua a zonas habitadas empujó los vectores hacia ellas y facilitó las epidemias de Puerto Esperanza en Misiones, y Porcelana-Carmelitas en Salta. La reducción o movimiento de animales silvestres, fuentes de alimento para los flebótomos, habría contribuido al pico de casos humanos en Alberdi, Tucumán, y Bella Vista, Corrientes.
En todos los casos la circulación de parásitos debió ocurrir antes del brote, y debió seguir después de él, según el ciclo natural vector-reservorio. Por eso, los casos esporádicos en humanos seguirán ocurriendo cada vez que una persona sea picada por un vector infectado en forma accidental. Las epidemias volverán a producirse cada vez que actividades humanas pongan en riesgo a un sector de la población, epidemias limitadas en espacio y duración por la biología de los vectores.
El flebótomo Lutzomyia neivai pertenece a una de las especies que habrían colonizado ambientes rurales y periurbanos en los últimos cincuenta años, lo que junto con cambios del volumen de lluvias, migraciones de población y modificaciones en el uso de la tierra, así como la presencia de otras especies de vectores que sirven de nexo en el ciclo silvestre, podría explicar el aumento de leishmaniasis cutánea en el cono sur de América a partir de la década de 1980. Desde 2004, se han capturado vectores, aunque no se ha registrado leishmaniasis, en Santa Fe, Entre Ríos y el norte de Córdoba, con lo que se fue extendiendo progresivamente la frontera de riesgo hacia el sur.
Leishmaniasis visceral en la Argentina:
una epidemia anunciada
Esta forma de la enfermedad está establecida en por lo menos cinco regiones del mundo, en las que los factores biológicos, ecológicos, epidemiológicos y socioeconómicos son diferentes, lo mismo que su importancia para la salud pública. Por ello resulta muy difícil extrapolar información de una a otra o a nuevas regiones.
Una de las mencionadas regiones es el nordeste del Brasil, donde la mayor parte de los casos ocurrían en áreas rurales. En las décadas de 1970 y 1980, con las migraciones internas, los vectores, los reservorios caninos y los humanos comenzaron a desplazarse hada el centro y el sur del país, y se produjeron brotes urbanos que ascendieron, en promedio, a 3300 casos por año, con un 6 a 8% de muertes. La leishmaniasis visceral alcanzó el estado de Mato Grosso do Sul hacia 2000. En 2002 se registró un caso en el Paraguay, donde para 2007 se registraban setenta casos por año, la mayoría en Asunción y el departamento Central.
Ante ese panorama, en la Argentina el Programa Nacional de Leishmaniasis puso en vigencia medidas de prevención consistentes en vigilar las áreas más vulnerables de la frontera norte para detectar la aparición del insecto Lutzomyia longipalpis, vector de la leishmaniasis visceral. Entre más de 250.000 flebótomos identificados en :rece provincias desde 1990, sólo se habían encontrado unos pocos ejemplares de dicha especie en 2000, en Corpus, Misiones, cerca del único sitio en que se registró una captura del insecto en 1953. En diciembre de 2004 se atrapó al vector en algunos barrios de Clorinda-Puerto Pilcomayo, separados apenas por un estrecho brazo de río de aquellos sitios del Paraguay en los que se verifica transmisión activa de leishmaniasis visceral.
Este hallazgo hizo aconsejable elevar el nivel de alerta e incorporar en el área de riesgo la vigilancia de casos humanos y caninos. La experiencia de otros países había demostrado que luego de la aparición del vector se produce un brote de casos caninos y después uno menos numeroso de casos humanos. Y, efectivamente, así sucedió en 2006: en una vivienda urbana de Posadas se presentó el primer caso de leishmaniasis visceral humana, producido por el parásito Leishmania infantum con presencia de Lutzomyia longipalpis y perros infectados en el entorno del enfermo. La enfermedad ya se estaba transmitiendo en territorio argentino: había comenzado una nueva etapa de su historia.
Entre febrero y marzo de 2007 se estudió la distribución del vector en Posadas-Garupá, y se encontró Lutzomyia longipalpis en el 42% de los 305 patios de viviendas en que se colocaron trampas, aunque sólo en poco más del 5% de los sitios se capturaron más de treinta vectores por noche. En las ciudades, aunque muchos sitios tienen posibilidad de ser colonizados, en pocos existe alto riesgo de transmisión en un momento determinado. Los vectores se concentran en islas de alta abundancia, favorecidas por la presencia de arbolado, gallinas y perros.
Ese tipo de islas también se observó en Clorinda, donde la distribución concentrada de vectores en 2007 fue semejante a la observada en 2004, pero la dispersión de perros con leishmaniasis visceral era mucho mayor debido al tránsito de canes infectados. El mismo fenómeno de dispersión del vector y de migración humana con perros infectados, que generó el avance de la leishmaniasis visceral del norte al sur del Brasil, se produjo en la Argentina: en diciembre de 2008 el parásito Lutzomyia longipalpis y la presencia de canes enfermos fueron constatados en Monte Caseros, en el sur de la provincia de Corrientes.
Diferente fue lo ocurrido en La Banda, Santiago del Estero, en 2007 y 2008. Allí hubo cuatro casos humanos, producidos por el parásito Leishmania infantum, y seis casos caninos. Los flebótomos encontrados no eran de la especie Lutzomyia longipalpis. A partir de esas constataciones, se ha postulado que podría tratarse de una forma no epidémica de leishmaniasis visceral, con casos aislados, transmitida por vectores que no
pueden mantener en el tiempo su ciclo de vida en el ecosistema chaqueño. Quizá esos casos estén asociados a otros registrados desde 1922 en diferentes provincias del norte.
El mayor riesgo se encuentra en la rápida dispersión de la leishmaniasis visceral en el medio urbano. Las drogas para uso humano no se deben utilizar en animales domésticos, por el riesgo de generar parásitos resistentes al tratamiento, y no hay terapias ni vacunas de efectividad comprobada para la leishmaniasis visceral canina. Aunque mejore su estado físico, la mayor parte de los animales siguen proporcionando parásitos a los vectores.
A mediados de 2009, tres años después de la confirmación de la leishmaniasis visceral en territorio argentino, un poco más de cincuenta personas, de las que cinco fallecieron, se habían enfermado en tres provincias (Misiones, Santiago del Estero y Corrientes).
Algunas conclusiones
Las leishmaniasis cutánea y mucosa, presentes en el país por lo menos desde comienzos del siglo XX, se expandieron en la década de 1980 con brotes rurales y periurbanos en nueve provincias en las que se constató transmisión, y en tres más en que se verifica la presencia del vector. La leishmaniasis visceral se instaló en medio urbano en la Argentina en 2006, con casos autóctonos, humanos y caninos, en cuatro provincias. Se constata en estos momentos que continúa la dispersión de vectores y de perros infectados que actúan como reservorios.
Los cambios climáticos y los factores asociados con la biología de los vectores contribuyeron al aumento de riesgo de leishmaniasis en la Argentina, a cuyo incremento también contribuyó -y en forma marcada- la acción humana. Desde la deforestación para la leishmaniasis cutánea a la tenencia de animales domésticos para su forma visceral; desde los cambios de uso de la tierra y del agua hasta los movimientos de población, pasando por el manejo de los patios de las viviendas, la gente ha precipitado la adaptación de vectores silvestres al medio doméstico, ha incorporado sangre humana y de animales domésticos a la dieta del insecto, y ha proporcionado nuevos reservorios para el parásito.
El estudio de las leishmaniasis muestra una tendencia al incremento de casos. La lucha contra los vectores con insecticidas da resultados en el corto plazo, pero a la larga es de poca efectividad. El tratamiento de la enfermedad actúa sobre una persona que ya la contrajo, y los tratamientos alternativos no siempre funcionan, mientras que las vacunas están aún en etapa experimental. Es predecible que la investigación biomédica proporcione nuevas herramientas, pero sólo entendiendo la incidencia de la conducta humana, individual y colectiva se podrá enfrentar con mayores posibilidades de éxito el desafio de enfermedades como las leishmaniasis.
--------------------------------
Lecturas sugeridas
Tres fuentes confiables de información sobre leishmaniasis son las páginas web de la Organización Mundial de la Salud:
(http://www.who.int/topics/leishmaniasis/en/index.html. la Organización Panamericana de la Salud.)
(http://www.paho.org/spanish/ad/dpc/cd/leishmaniasis.htm) y los Centers for Disease Control and Prevention de los Estados Unidos
(www.cdc.gov/ncidod/dpd/parasites/leishmania/factsht_leishmania.htm).
Enfoques médicos se pueden encontrar en: http://emedicine.medscape.com/article/998804-overview y en:
http://www.nim.nih.gov/medlineplus/ency/article/001386.htm. También son recomendables documentos de la Fundación Mundo Sano (http://www.mundosano.org/documentos/monografias/Monografía 2.pdf y http://www.mundosano.org/documentos/monografias/Monografía 6.pdf.

Patricio J Garrahan
Doctor en medicina, UBA.
Profesor emérito, UBA.
Investigador superior, Conicet.

Oscar Daniel Salomón
Doctor en ciencias biológicas, UBA. -Investigador independiente, Conicet.
Director del Centro Nacional de Endemo-Epidemias, Ministerio de Salud.
Coordinador Programa Nacional de Leishmaniasis.
odanielsalomon@gmail.com
|
|



