El
Quinto Jinete
El Comité de Redacción de Acta
Bioquímica Clínica Latinoamericana
ha seleccionado este artículo publicado en la Revista Industria
& Química
Nº 353 - 2006, para su difusión a través de FABA
Informa.
“Vi otra bestia que subía
de la tierra y tenía dos cuernos semejantes a los de un cordero,
pero hablaba como un dragón.”
Apocalipsis 13-14
Mario R. Féliz
Instituto de Investigaciones Fisicoquímicas
Teóricas y Aplicadas (INIFTA). Universidad Nacional de La
Plata. E-mail:
mfeliz@ciudad.com.ar
Introducción
En la última década del siglo XV, un año después
del descubrimiento de América, nacía en Suiza Auroleus
Phillipus Theofrastus Bombastus von Hohenheim, mejor conocido como
Paracelsus [1]. Este alquimista, durante los 48 años de su
existencia breve, se dedicó a la ciencia de los venenos.
Lo hizo de tal suerte, que sus trabajos lo convirtieron en el padre
de la toxicología moderna.
Un resumen de su legado, aún vigente, lo encontramos en un
comentario suyo, convertido en lema de la disciplina: “Todas
las sustancias son venenos; no hay una que no lo sea. Es la dosis
correcta lo que diferencia el veneno del remedio”.
El sabio criterio de Paracelsus es frecuentemente olvidado, y cada
vez que se descubre la toxicidad de una nueva sustancia, rápidamente
surgen voces exigiendo fijar nivel cero para su emisión.
Este criterio es obviamente equivocado, innecesario y podría
ser peligroso.
El oxígeno (O2) es imprescindible para la vida de muchos
integrantes de la biota actual. Sin embargo, es terriblemente tóxico
para la todavía abundante, e imprescindible, biota anóxica.
Si el sistema regulatorio de la Tierra [2] fallara y la cantidad
de oxígeno subiera por encima de los niveles actuales, la
vida para los respiradores de oxígeno (O2) se complicaría.
Si por el contrario, su nivel disminuyera por debajo del 21 % del
aire que respiramos, también estaríamos en problemas.
Respirar oxígeno es quizás lo que pone límite
a la vida de la mayoría de los animales. Aun en las ideales
condiciones actuales, el oxígeno muestra su toxicidad. Especies
muy reactivas, derivadas de ese elemento, son generadas en el organismo:
ión peróxido, ión superóxido y otras
especies de oxígeno activadas. Todas ellas son de una muy
alta toxicidad y, aunque el organismo humano posee mecanismos para
su destrucción, aquellas igualmente ejecutan su deletéreo
trabajo, incluyendo el de carcinogénesis. Sin embargo, fijar
a nivel cero el oxígeno para prevenir el cáncer sería
algo totalmente equivocado, un grave error sin duda.
Emerge la bestia
El incidente ocurrió en 1976, en Seveso, al norte de Italia.
Se debió a la explosión de un reactor durante la producción
de 2, 4, 5-triclorofenol [3]. Se liberó allí una nube
tóxica que contenía cerca de 3.000 kg de varias sustancias
químicas, entre las cuales había entre 30 y 100 kg
de dioxina tetraclorada.
Fue aquel episodio el que, probablemente, despertó la alarma
y dio origen al relato del Quinto Jinete, la dioxina, capaz de iniciar
un ciclo de catástrofes que completaría, seguramente,
el buen trabajo realizado hasta entonces por los otros cuatro jinetes
bíblicos.
Desde entonces, incentivada por otro par de hechos accidentales,
la búsqueda de dioxina obtuvo resultados definitivamente
positivos, hallándola en casi todas partes. De tal forma
se desarrollaron los acontecimientos que algún científico
americano escribió [4], en 1998: “La exposición
de una gran proporción de la población de U.S., a
la dioxina del “background” en los niveles no actuales,
está ya, probablemente, causando una crisis sanitaria nacional”.
¿Qué son las dioxinas?
<
Figura 1.- Dioxina Teraclorada
Son compuestos orgánicos aromáticos (poseen anillos
formados por átomos de carbono [C] unidos entre sí
con uniones simples y dobles). En estas, dos de tales anillos están,
a su vez, unidos por dos átomos de oxígeno [O]. Si
además los átomos de hidrógeno, unidos a los
carbonos, son sustituídos por átomos de cloro [Cl],
tenemos las dioxinas cloradas.
La figura nos muestra la dioxina tetra clorada. En los carbonos
donde no hay CI, hay hidrógenos [H], excepto en aquellos
carbonos que son compartidos por dos anillos.
Esta dioxina, poli-clorada, cuyo nombre es 2, 3, 7, 8 – tetraclorodibenzo
- p- dioxina (2, 3, 7, 8-TCDD), donde los números indican
la posición de los átomos de cloro en la molécula,
es un compuesto tóxico y cancerígeno. No hay evidencia
de que induzca cáncer en humanos. Sin embargo, de su probada
capacidad para producirlo en animales de laboratorio se le atribuye
la propiedad de generarlo en las personas. Sin embargo, cuando el
número de átomos de cloro presentes en la molécula
disminuye, su toxicidad cae drásticamente a cero [5].
La dioxina penta-clorada (1,2,3,7,8-PCDD) tiene la misma toxicidad
que la 2,3,7,8-TCDD. No obstante, si aumenta el número de
Cl, aún más, la toxicidad disminuye, siendo para la
dioxina con ocho átomos de cloro (OCDD) 10.000 veces menor
que la atribuida a la TCDD.
Existe otro grupo de compuestos parientes, derivados del dibenzo
furano. Esta es una sustancia parecida a la dioxina, pero con un
solo “puente” oxígeno. Entre ambos grupos, dioxinas
y furanos clorados, suman más de doscientos congéneres.
Entonces, cuando hablamos de dioxinas nos referimos a todos estos
compuestos.
Las dioxinas poli-cloradas son hidrófobas (no se encuentran
cómodas en medio del agua) por lo cual, en ríos y
lagos, se refugian en el sedimento donde encuentran un medio hidrófugo
confortable. Tal ubicación hace que, en principio, aunque
el agua no contenga dioxinas, éstas sean incorporadas por
la biota del sedimento y luego por los peces que se alimentan de
ella. En los peces, debido a su carácter hidrófobo,
las dioxinas se acumularán en las grasas y algunos órganos
como el hígado. Es a través de la ingesta frecuente
de peces que el hombre puede incorporarlas a su organismo.
¿De dónde provienen las dioxinas?
<
TABLA 1.- Fuentes de emisión
de Dioxinas en EE. UU.
Categoria
|
1987
% del total |
1995
% del total |
2002/04
% del total |
Incineración
|
82 |
54 |
3 |
Quema domiciliaria de basura
|
4 |
29 |
56 |
Procesos metalurgicos
|
6 |
9 |
3 |
| Hornos de cemento |
0.94 |
5 |
2 |
Tratamiento de barros cloacales
|
0.55 |
2 |
6 |
Pulpa de celulosa y papel
|
2.67 |
0.71 |
1 |
| Quema de carbón para obtener electricidad |
0.36 |
1 |
5 |
| Quema industrial de madera |
0.19 |
0.85 |
2 |
| Quema domiciliaria de madera |
0.64 |
1 |
5 |
| Vehículos diesel |
0.20 |
1 |
3 |
| Otros |
0.98 |
3 |
9 |
| Total (g-TEQ) |
13.949 |
3.252 |
1.106 |
Si, como hemos visto, las dioxinas se encuentran en todas partes:
¿de dónde provienen, entonces?.
La EPA (Environmental Protection Agency - USA) ha realizado un inventario
de las fuentes de tales compuestos y ha cuantificado la contribución
que hace cada una. En la tabla 1 pueden verse las principales fuentes
de dioxinas y como, a raíz de algunas regulaciones, la producción
total ha ido disminuyendo con los años [6]. Además,
se observa que el 70% proviene de actividades no industriales y
que, en el estimado para 2004, la industria de la celulosa y papel
sólo contribuye con 1%. Esto significa que del total de dioxinas
producidas, esta actividad aporta apenas 15g- TEQ, en 2000, cuando
en 1987 su aporte era de 372 g- TEQ. En la actualidad, tal contribución
ha caído aún más, a medida que la industria
se ha reconvertido, eliminando el blanqueado de la pulpa con gas
cloro (Cl2).
Por otra parte, si se tiene en cuenta que los incendios forestales,
en USA, aportan una cantidad superior ala proveniente de todas las
otras fuentes, la contribución de todas las industrias no
superaba e115% del total, en el año 2004.
Del análisis de estos surgen, evidentes, dos conclusiones:
a) el total de dioxinas de origen industrial es menor comparado
con las otras fuentes y b) el aporte de la industria de la celulosa
es bajo y tendiendo a cero, siguiendo el ritmo de aplicación
de los nuevos métodos de blanqueado de pulpa.
¿Cómo se generan las dioxinas?
Para su producción hacen falta sustratos adecuados (Una estructura
orgánica compleja: lignina, madera, papel o plásticos)
y una fuente proveedora de átomos de cloro (Cl), como Cl2,
NaCl (cloruro de sodio = sal en de cocina), cloruro de hidrógeno
(HCl) o el plástico PVC (cloruro de polivinilo). A ello hay
que agregar una temperatura suficientemente alta como la que se
obtiene al quemar madera, papel o plásticos.
En el proceso de blanqueado de pulpa con cloro tenemos todos los
componentes necesarios.
El proceso de blanqueado implica la destrucción de la lignina,
por oxidación con cloro. La lignina es un polímero
complejo que es degradado a compuestos separables, por lavado, de
la fibra de celulosa. En este proceso la mitad de los Cl0 oxidan
la lignina y se convierten en iones cloruro (Cl1-).
Lignina + Cl° ? productos
de oxidación + Cl1-
En tanto la otra mitad de los Cl0 reemplazan hidrógenos
en algunas moléculas aromáticas (el proceso se llama:
sustitución electrofílica) y dan origen a las indeseables
TCDD o TCDF. Por ejemplo:
Dioxina no clorada +
4 Cl0 ? 2,3,7,8-TCDD
Si se disminuye la cantidad de átomos de cloro
en el reactor de blanqueado, es posible impedir la formación
de dioxinas tetra o penta cloradas. Sólo se forman, entonces,
compuestos mono-, di- ó tri-clorados que tienen dos ventajas:
a) no son tóxicos y b) se degradan con cierta rapidez en
el medio ambiente. Es bueno aclarar que la presencia de cloro en
los anillos bencénicos produce el efecto de disminuir su
reactividad. Así, al aumentar el número de Cl en la
molécula, las dioxinas se hacen más resistentes a
la degradación natural.
Para disminuir la formación de dioxinas tetracloradas a niveles
por debajo de los valores permitidos, la industria celulósica
ha reemplazado el gas Cl2 por el gas ClO2 (dióxido de cloro),
en el proceso de blanqueado.
¿Cómo es posible lograr ese propósito con una
sustancia que también tiene cloro? Pues, es posible porque
el ClO2 tiene una capacidad de oxidación varias veces mayor
y, además, porque el mecanismo de acción hace que
la posibilidad de tener Cl (cloro elemental) en el medio es mucho
menor.
Al oxidar la lignina el dióxido de cloro se convierte en
el ión clorito:
Lignina + ClO2 ? productos de oxidadación
de la lignina
+ ClO21- (clorito)
Otros productos de la reducción del ClO2 (dióxido
de cloro) son el Cl1- (ión cloruro) y el ión hipoclorito
(CIO1-). Este último se encuentra en equilibrio con otras
especies:
ClO1- + H+ ? ClOH
ClOH + CIH ? Cl2 + H2O
De esta manera tenemos presentes las especies ClOH
(ácido hipocloroso) y Cl2 que tienen la capacidad de clorar.
Sin embargo, si se mantiene el medio alcalino la especie predominante
será ClO1- que es oxidante y no clorante. Se disminuye así,
aún más, la posibilidad de tener poli-clorados.
Por otra parte, si el proceso de blanqueado con ClO2 es precedido
de un predeslignificado con oxígeno o H2O2 se disminuye la
cantidad de óxido de cloro necesario y por consiguiente,
la posibilidad de formación de órganoclorados.
Esta descripción, aunque ultra simplificada, no deja de ser
pura teoría. La única forma de asegurarse de que lo
que decimos es cierto es ver qué ha ocurrido con el contenido
de dioxinas en los efluentes líquidos emitidos por las plantas
de pulpa de celulosa.
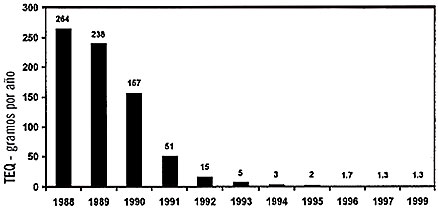
Veamos en la siguiente figura datos sobre Canadá. En ella
se observa cómo la cantidad de dioxinas ha disminuido a medida
que las plantas de celulosa han ido reemplazando el Cl2 por el ClO2.
Actualmente en Canadá y USA esos niveles se mantienen por
debajo de los niveles permitidos.
<
CANADA: Eliminación de los cursos de agua en las plantas
de celulosa
Para completar el cuadro podemos agregar que, en USA, los avisos
de peces conteniendo dioxinas fueron decreciendo con los años
y, desde 2004, no se recibe ningún aviso. Este hecho es muy
importante ya que, a pesar de la persistencia de los aromáticos
policlorados, estos igualmente desaparecen progresivamente de los
peces rompiendo la cadena de bioacumulación.
En definitiva, no parece que vayan a cumplirse las predicciones
apocalípticas de hace algunos años y que en estos
días se repiten, por aquí, como si nada hubiese cambiado.
Muy por el contrario los resultados de la investigación científica
y tecnológica, las correctas regulaciones y los adecuados
controles muestran que se pueden mantener los efectos, de algunas
actividades humanas que pudieron ser peligrosas, en niveles francamente
inofensivos.
Terminemos recordando los dichos del panel de expertos, encabezado
por el biólogo Wayne Dwernychuk, que revisara, recientemente,
el posible impacto ambiental de las plantas de Fray Bentos: "El
panel no encontró ninguna razón que diera sustento
a las predicciones de daño ambiental catastrófico
en el entorno receptor, que han sido presentadas por varios actores".
Referencias Bibliográficas
[1] www.alchemylab.com
[2] Las Edades de Gaia, James Lovelock. Ed. Metatemas.
[3] Polychlorinated dibenzo-p-dioxins (PCDD), dibensofurans (PCDF)
and polychlorinated biphenyls (PCB): main sources, environmental
behaviour and risk to man and biota. M. de Souza Pereyra. Química
Nova, 2006, 27(6).
[4] Jonathan Campbell. ATSDR 1998.
[5] ATSDR 1997, 13(6). Varios autores.
[6] DioxinFacts.com
|
|


