|
|||
|
| ARG |
Tumores sólidos: Análisis genómico en el laboratorio
La frecuencia de los procedimientos de diagnóstico que utilizan el ADN libre de células (cfDNA) del plasma humano ha aumentado drásticamente en los últimos años. Aquí, se confirma que los fragmentos de cfDNA derivado del tumor son similares en la distribución de tamaño a cfDNA derivado de los tejidos normales. Por lo tanto, es probable que los procedimientos de recolección optimizados para muestras de donantes sanos sean aplicables al diagnóstico y monitoreo de muchos tipos diferentes de cáncer. Se verifica que la distribución y las secuencias de ADN de los sitios de fragmentación en cfDNA tanto de la línea madre germinal normal y el cfDNA derivado de tumores no son aleatorios. Una amplia encuesta de cfDNA de donantes sanos sugiere que los individuos promedio poseen ~ 6 ng de cfDNA por ml de plasma. Es importante destacar que el cfDNA presente en muestras de plasma que se recogieron inicialmente como sangre entera en tubos de EDTA- K2 y posteriormente se procesaron por centrifugación es estable durante varios días a temperatura ambiente. Esta observación tiene el potencial de reducir significativamente el costo y la complejidad logística de enviar muestras clínicas desde el sitio de recolección a los centros competentes en análisis de diagnóstico. Finalmente, las muestras de plasma recogidas con dispositivos de colecta de plasma de alto volumen poseen cantidades abundantes de cfDNA. Dado que la cantidad de cfDNA analizado es directamente proporcional a la sensibilidad de los ensayos diagnóstico, este método de recolección de plasma, cuando está disponible, podría permitir un seguimiento de la enfermedad post-tratamiento altamente sensible y la detección temprana del cáncer en individuos de riesgo. 1: Medina Diaz I, Nocon A, Mehnert DH, Fredebohm J, Diehl F, Holtrup F. Performance of Streck cfDNA Blood Collection Tubes for Liquid Biopsy Testing. PLoS One. 2016 ;11(11):e0166354. 2: Wong FC, Sun K, Jiang P, Cheng YK, Chan KC, Leung TY, Chiu RW, Lo YM. Cell-free DNA in maternal plasma and serum: A comparison of quantity, quality and tissue origin using genomic and epigenomic approaches. Clin Biochem. 2016;49(18):1379-1386. 3: Norton SE, Lechner JM, Williams T, Fernando MR. A stabilizing reagent prevents cell-free DNA contamination by cellular DNA in plasma during blood sample storage and shipping as determined by digital PCR. Clin Biochem. 2013 Oct;46(15):1561-5. 4: Norton SE, Luna KK, Lechner JM, Qin J, Fernando MR. A new blood collection device minimizes cellular DNA release during sample storage and shipping when compared to a standard device. J Clin Lab Anal. 2013 Jul;27(4):305-11. 5: Parpart-Li S, Bartlett B, Popoli M, Adleff V, Tucker L, Steinberg R, Georgiadis A, Phallen J, Brahmer J, Azad N, Browner I, Laheru D, Velculescu VE, Sausen M, Diaz LA Jr. The Effect of Preservative and Temperature on the Analysis of Circulating Tumor DNA. Clin Cancer Res. 2017 May 15;23(10):2471-2477. Español 1: Olivier Gómez C, Carballido Rodríguez J. Células tumorales circulantes: aislamiento, cuantificación y relevancia de su traslación a la práctica asistencial. Actas Urol Esp. 2010;34(1):3-5. 2: Tolosa A. Huellas moleculares en el ADN libre en sangre informan sobre su origen celular. Cell. 2016;164(1-2):57-68. doi: 10.1016/j.cell.2015.11.050. 3: Hernández MC. Micrometástasis en tumores sólidos: ¿qué son y qué significa su detección por métodos de inmuno histoquímica? Rev Inst Nal Cancerol (Mex). 2000; 46 (3):207-14.
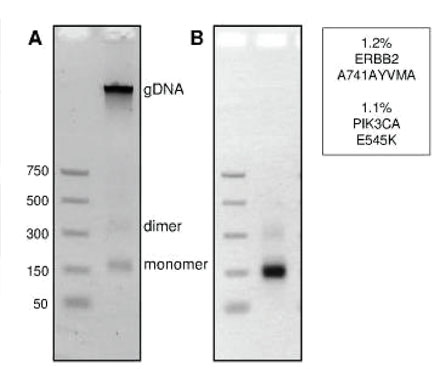
(A) El ADN purificado a partir de plasma consiste a menudo en fragmentos de ADN cortos de ADN nucleosómico como monómero, dímero, trímero, y fragmentos de gDNA de alto peso molecular. (B) El ADNc extraído del plasma de un paciente con cáncer pulmonar de células no pequeñas (NSCLC, por su sigla en ingles) parecía ser exclusivamente fragmentos nucleosómicos, y se detectaron mutaciones específicas de tumor mostradas en el gel en el análisis genómico resultante. De la comparación de las figuras A y B: indicar dentro de qué rango de PM (peso molecular) está el cfDNA extraído del plasma del paciente con NSCLC. Le informamos que se le obsequiará un CD con material bibliográfico a elección de un listado que tenemos disponible, a los primeros que nos hagan llegar su respuesta correcta al correo electrónico bibliote@fbpba.org.ar Agradecemos por este medio a los profesionales que han participado y respondido las actividades publicadas en ediciones anteriores. Jefe Responsable del Sector: Dra. Nilda Fink Consulte nuestros servicios |
||
| Subir | ^ |
Tumores sólidos: Análisis genómico en el laboratorio |