El Comité
de Redacción de Acta Bioquímica Clínica Latinoamericana
ha seleccionado este artículo publicado en la revista “Investigación
y Ciencia”, junio de 2003, para su difusión a través
de FABA Informa.
Robert Langer
A través de los pulmones
La vía pulmonar representa una importante oportunidad, pero también
un desafío en el tratamiento de enfermedades pulmonares y como
sistema de administración de fármacos para el tratamiento
de enfermedades de cualquier otra parte del cuerpo. Los pulmones constan
de sáculos microscópicos, los alvéolos, unidos directamente
a los vasos sanguíneos. Durante la respiración, el oxígeno
llega a la sangre a través de los alvéolos y se elimina
el dióxido de carbono, producto de desecho. Por un mecanismo similar
pueden alcanzar el torrente sanguíneo fármacos en forma
de aerosol que contengan moléculas mayores, proteínas por
ejemplo. Hasta el momento ha sido difícil diseñar sistemas
de inhalación que produzcan una cantidad suficiente de partículas
de aerosol de un tamaño tan pequeño como para penetrar de
manera profunda en el pulmón sin desperdiciar el fármaco.
La mayoría de los inhaladores tradicionales, como los que se utilizan
en el tratamiento del asma, administran menos de un 10 por ciento de su
contenido. Los macrófagos pulmonares, células del sistema
inmunitario, pueden eliminar la mayoría de los fármacos
de forma rápida.
Son muchos los investigadores y compañías que trabajan en
el perfeccionamiento de los sistemas de inhalación y buscan aerosoles
extremadamente finos. Aradigm de Hayward, California, ha desarrollado
un sistema para formulaciones líquidas. El fármaco atraviesa
unos filtros que se pueden programar para administrar dosis específicas.
En Nectar Therapeutics de San Carlos, California, mezclan polvo seco con
aire comprimido y se forma una nube de aerosol de pequeñas partículas
que alcanzan las regiones más profundas de los pulmones. Ambas
compañías están realizando también ensayos
con insulina que no requieran el uso de inyecciones.
A mediados de la década de los noventa, los científicos
no prestaban demasiada atención a las partículas de aerosol.
David A. Edwards, docente hoy en la Universidad de Harvard, razonó
que si se disminuía la densidad de las partículas a la par
que se incrementaba su tamaño y su porosidad, su tendencia a la
agregación debía reducirse. Así, un inhalador pequeñísimo
y simple debía bastar para que el aerosol llegara hasta los pulmones.
Considérese, por ejemplo, la diferencia entre balones de fútbol
mojados y granos de arena húmedos. Es obvio que los últimos
tienen una tendencia a adherirse entre sí mucho mayor que los primeros.
Al aumentar el tamaño de las partículas, Edwards pensó
que también podría conjurar su eliminación por los
macrófagos pulmonares, cuya tendencia es la de rodear las micropartículas
y destrozar los fármacos. Edwards y otros científicos, entre
ellos el autor, demostraron que una sola dosis de insulina formulada en
un aerosol de partículas grandes puede durar hasta cuatro días
en los pulmones de animales. El método se está ensayando
en humanos con diversos fármacos en Alkermes, Cambridge, Massachusetts,
en colaboración con varios laboratorios farmacéuticos.(Ver
imagen)
Microchips inteligentes
Los sistemas inteligentes de administración de fármacos
revisten especial interés. En respuesta a señales químicas
en el organismo, liberarían fármacos de forma que su concentración
en el organismo se mantuviera dentro de un nivel terapéutico deseado.
Hace unos años, cuando el autor estaba viendo un programa de televisión
sobre la fabricación de chips de silicio para computadores, concibió
la posibilidad de aplicarlos a la administración de fármacos.
Junto con Michael J. Cima, experto en procesamiento de cerámicas
del MIT, convenció a John T. Santini Jr., de la Universidad de
Michigan en Ann Arbor, para que estudiara esta posibilidad como proyecto
de investigación de verano. Santini, que acabó realizando
el doctorado en el MIT, desarrolló un método para crear
microchips de silicio que contuvieran una serie de reservorios rellenables
con medicación y que estuvieran recubiertos por un fino pan de
oro. La aplicación de una corriente eléctrica de un volt
a uno o más de los pocitos disuelve el recubrimiento áureo
y libera el fármaco. Santini preside ahora MIcroCHIPS en Bedford,
que está desarrollando el método para su ensayo en humanos.
Controlar las dosis
Microchip implantable
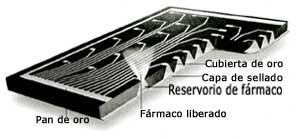
Retos: mantener niveles terapéuticos
estables del fármaco en el organismo, al tiempo que se
evita la necesidad de repetir la administración.
Soluciones: microchips implantables con depósitos
de medicación, recubiertos por un pan de oro, que se disuelve
al producirse una pequeña descarga eléctrica y libera
el fármaco cuando es preciso.
|
Los microchips se podrían implantar por debajo de la piel, en la
médula espinal o en el cerebro para liberar fármacos analgésicos
o aplicar quimioterapia contra el cáncer.
Los estudios en animales de James Anderson, y sus colaboradores, de la
Universidad Case Western Reserve, han demostrado que los materiales de
los microchips no son incompatibles con tejidos vivos y que es poco probable
que produzcan efectos secundarios. Los sistemas basados en chips, que
incluirían una pila pequeña, serían sencillos de
manejo y podrían controlar de forma precisa la cantidad de fármaco
que el paciente consume. Los datos facilitados por estos sistemas podrían
descargarse en un computador en el domicilio, en la consulta del médico
o en el hospital y permitirían un registro actualizado de la historia
farmacológica del paciente. ChipRx, de Lexington, Ky., está
desarrollando sistemas implantables sensibles a la concentración
medicamentosa.
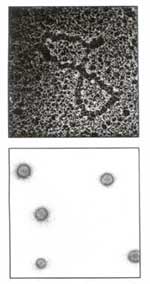 El
plasmido El
plasmido
(arriba) debe penetrar en la célula
y empezar a funcionar para poder acometer la terapia génica.
La mayoría de los tests de terapia génica aplicados
a las personas se han servido de virus vectores que introducían
el material génico en el interior celular. Un proceso no exento
de riesgos. Por esa misma razón, se investiga ahora el método
de encapsulamiento polimérico (abajo). |
Se espera con ansiedad el día en que cualquier fármaco pueda
administrarse en el momento preciso en la dosis apropiada en cualquier
parte del organismo de forma específica y eficiente.
Bibliografía complementaria
• DRUG DELIVERY AND TARGETING. Robert Langer, en Nature, vol. 392
(suplemento), págs. 5-10; 30 de abril de 1998.
• DRUG DELIVERY: DRUGS ON TARGET. Robert Langer,
en Science, vol. 293, págs. 58-59; 6 de julio de 2001.
• ULTRASOUND-ASSISTED INSULIN DELIVERY AND NONlNVASIVE
GLUCOSE SENSING. Joseph Kost, en Diabetes Technology and Therapeutics,
volumen 4, nº 4, págs. 489-497; 2002.
Administración de genes
El auténtico desafio de la terapia génica reside en la posibilidad
de introducir nuevo material génico en el interior celular
Tal como ha afirmado Inder M. Verma, del Instituto Salk
para Estudios Biológicos de San Diego, son tres los desafíos
de la terapia génica: administración, administración
y administración. Para introducir un gen en el cuerpo, hay que
concentrar el ADN correspondiente para que la célula lo pueda incorporar.
Pero eso no es todo: debe también protegerse al gen de las enzimas
celulares, transportarlo hasta el núcleo celular y, luego, liberarlo
en forma activa. Durante años, se han venido empleando virus por
vectores, verdaderos caballos de Troya que introducen disimuladamente
genes extraños en las células. Estos virus, incluso desactivados,
conllevan un riesgo, como se comprobó en 1999 con la trágica
muerte de Je sse Gelsinger, el voluntario de un ensayo sobre terapia génica.
Al tiempo que se trabaja para conocer y reducir los peligros asociados
a vectores víricos en la terapia génica, se buscan formas
alternativas para transportar genes basadas en polímeros o en lípidos.
Mark E. Davis, del Instituto de Tecnología de California, ha obtenido
resultados esperanzadores con B-ciclodextrinas catiónicas (CD),
polímeros con carga positiva.
Davis escogió las ciclodextrinas catiónicas por una triple
razón: escasas toxicidad, incapacidad inmunógena y solubilidad
en agua. Al principio intentó condensar el ADN únicamente
en partículas de ciclodextrinas de tamaño nanométrico,
pero esta combinación resultaba inestable cuando se administraba
a animales. Con su colaboradora Suzie Hwang Pun, Davis decidió
alterar la superficie de las partículas de ciclodextrinas mediante
adición de polietilenglicol (PEG) conjugado con adamantano. La
modificación producía nanopartículas de ciclodextrinas
y ADN de tamaño uniforme que se resistían a conformar agregados
inútiles con proteínas del suero.
La adición de los compuestos de polietilenglicol en la superficie
de las partículas les proporcionó verdaderos ganchos químicos
mediante los que aprehender otras moléculas y administrar los genes
a determinados tipos celulares. Insert Therapeutics, de Pasadena, California,
fundada por Davis y en la que trabaja actualmente Pun, está realizando
ensayos para comprobar si estos complejos se pueden utilizar en el tratamiento
de algunos tipos de cáncer y enfermedades hepáticas.
David M. Lynn, de la Universidad de Wisconsin en Madison, también
trabaja en el desarrollo de polímeros especializados como vectores
de terapia génica.
Lynn, antiguo becario posdoctoral en el laboratorio del autor en el MIT,
ha sintetizado una extensa serie o biblioteca de polímeros catiónicos
biodegradables llamados poliaminoésteres. En colaboración
con Daniel Anderson y David Putnam, Lynn ha fabricado cientos de tales
polímeros y ha desarrollado una serie de métodos para identificar
los más útiles en función de su capacidad de unión
del ADN, su solubilidad en el suero y su capacidad de penetrar en el interior
de las células. De esta manera, se han identificado una serie de
polímeros más eficientes que los vectores no víricos
habituales, como lipofectamina y polietilenamina.
Fred E. Cohen, de la Universidad de California en San Francisco, también
ha recurrido al método de la biblioteca.
En colaboración con Ronald Zuckerman, de los laboratorios Chiron,
Cohen ha sintetizado una nueva clase de polímeros, los peptoides,
oligómeros de glicina catiónicos con sustitución
N. Algunos de ellos condensan ADN en partículas de entre 50 y 100
nanómetros, aptos para penetrar en el interior celular.
Los lípidos también son útiles en la administración
de terapia génica, como demuestran los trabajos de Sung Wan Kim,
de la Universidad de Utah. Kim recubre el gen que se quiere administrar
con una vaina de estearilpolilisina que luego envuelve con lipoproteínas
de baja densidad. En estudios con conejos, él y a sus colaboradores
han logrado administrar el gen del factor de crecimiento vasculoendotelial
en miocardio dañado por falta de oxígeno, como sucede cuando
se obstruye un vaso sanguíneo. Kim se plantea comenzar un estudio
con pacientes con cardiopatía isquémica. Cifra su esperanza
en que el gen del factor de crecimiento vasculoendotelial estimulará
el desarrollo de nuevos vasos sanguíneos que aporten oxígeno
y nutrientes al miocardio afectado. |