En su aplicación, el fármaco
debe recorrer un largo camino desde el frasco de las pastillas hasta que
mitiga el dolor o alcanza el foco de infección. Se buscan procesos
novedosos para que la medicina llegue intacta allí donde se precisa.
El Comité de Redacción
de Acta Bioquímica Clínica Latinoamericana ha seleccionado
este artículo publicado en la revista “Investigación
y Ciencia”, junio de 2003, para su difusión a través
de FABA Informa.
El sencillo acto de tomar una pastilla es el principio
de un tortuoso laberinto para el medicamento. Debe superar, en primer
lugar, el estómago y llegar intacto al intestino, para luego atravesar
la pared intestinal antes de alcanzar la circulación sanguínea.
Instalado aquí, el hígado hará de filtro antes de
permitir que el fármaco continúe su viaje por el resto del
cuerpo. En las sucesivas estaciones, el compuesto deberá resistir
los ácidos gástricos, vencer membranas de barrera o defenderse
de enzimas diseñadas para trocearlo en fragmentos inservibles.
Los laboratorios farmacéuticos han ideado soluciones parciales
para allanar el camino de los compuestos hasta su destino. Pero no son
aplicables a todos los medicamentos. Una de las estrategias consiste en
recubrir las píldoras de una coraza resistente a los jugos gástricos,
que se disuelve cuando alcanza el intestino delgado, más alcalino.
Aun así, los medicamentos basados en proteínas (como es
el caso de la mayoría de los productos sintetizados con biotecnología)
deberán evitar también la actividad de las proteasas, enzimas
que actúan directamente sobre las proteínas y las dirigen.
Se puede proteger a las píldoras con sustancias específicas
(inhibidores de las proteasas) para facilitar su supervivencia; ello,
sin embargo, dificulta el paso a través de la pared intestinal.
Las píldoras con este recubrimiento resultan demasiado grandes
para penetrar en la sangre con la misma facilidad con que lo hacen los
medicamentos corrientes que, en general, se componen de micromoléculas.
Los revestimientos limitan, asimismo, el control sobre la farmacocinética
del medicamento, esto es, la velocidad con que llega al torrente circulatorio
y el tiempo que permanece almacenado en órganos y tejidos. Un fármaco
puede resultar tóxico tanto si alcanza grandes concentraciones
en sangre demasiado rápido, como si permanece en ella demasiado
tiempo. Por el contrario, puede tornarse ineficaz si se demora su entrada
en la circulación.
La administración parenteral de un medicamento, como las inyecciones,
ahorra los inconvenientes derivados de su paso por el tracto gastrointestinal,
pero muchos pacientes son reticentes a pincharse varias veces o a tener
que acudir a diario al médico. Desde hace veinte años se
vienen diseñando multitud de sistemas alternativos de administración
de medicamentos: sólo en EE.UU. la venta de medicamentos que se
administran a través de parches, implantes, inyecciones de preparados
de acción prolongada, geles tópicos, píldoras de
liberación controlada e inhaladores nasales o pulmonares exceden
los veinte mil millones de dólares al año.
Recientemente, la autoridad competente en EE.UU. en materia de medicamentos,
la Administración para la Alimentación y Fármacos
(FDA), ha aprobado la comercialización de dos buenos ejemplos:
Nutropin Depot y Gliadel. Nutropin Depot es un compuesto de microesferas
de polímeros degradables que libera somatotropina, la hormona del
crecimiento, durante semanas después de cada inyección.
Gliadel, en forma de sello, se implanta en el cerebro para la administración
directa de quimioterapia sobre un tumor. En Europa se dispone ya de endoprótesis
vasculares revestidas de polímeros para la liberación de
medicamentos específicos que han demostrado su valía en
la repermeabilización por angioplastia de arterias que presentan
obstáculos al flujo sanguíneo.
Se ha explorado cada rincón del cuerpo humano (piel, nariz, pulmones
e intestinos, entre otros) en busca de posibles puertas de entrada para
los fármacos y para el desarrollo de sistemas no invasivos de administración
de moléculas complejas.
Gracias a estos esfuerzos, se ha conseguido incrementar la capacidad de
absorción de un medicamento a través de la piel mediante
ultrasonidos y se ha recurrido a la nanotecnia para la fabricación
de microchips implantables que regulan la dosificación de principios
activos de forma precisa y programada. (Ver
imagen 1).
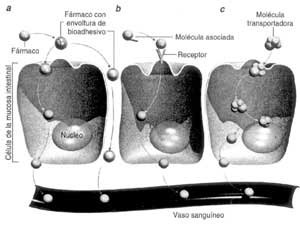 ATRAVESAR
EL INTESTINO: RETOS: Los ácidos gástricos y las enzimas
destruyen los fármacos antes de que puedan alcanzar su destino;
los medicamentos encuentran dificultades para atravesar la pared intestinal. ATRAVESAR
EL INTESTINO: RETOS: Los ácidos gástricos y las enzimas
destruyen los fármacos antes de que puedan alcanzar su destino;
los medicamentos encuentran dificultades para atravesar la pared intestinal.
SOLUCIONES: (a) Cubrir los fármacos con polímeros bioadhesivos
que se pegan a la pared intestinal y que penetran entre las células
intestinales; (b) asociar los fármacos a moléculas cuyos
receptores en el intestino facilitan que la medicina penetre en las células;
(c) unir fármacos a moléculas transportadoras que los introduzcan
en las células.
A traves de la pared intestinal
Para solucionar el problema del paso a través de la pared intestinal
se ha hecho un uso intensivo de las nuevas técnicas. Edith Mathiowitz
y su equipo, de la Universidad Brown, han logrado, con una. sustancia
adhesiva, un bioadhesivo, fabricar burbujas finísimas y colocar
en su interior proteínas de uso médico. Las burbujas pueden
penetrar en las células intestinales o colocarse por los intersticios
entre células. La bioadhesión (la adherencia de fármacos
administrados por vía oral a las membranas mucosas) tiene su origen
en los trabajos realizados en los años setenta y ochenta en los
laboratorios de Tsuneji Nagai, de la Universidad Hoshi de Tokio, Joseph
R. Robinson, de la Universidad de Wisconsin en Madison, y Nicholas A.
Peppas, de la Universidad Purdue. Hasta hace diez años se consideraba
que los bioadhesivos más prometedores eran polímeros hidrofílicos
e hidrogeles. De estos estudios los investigadores dedujeron que los materiales
idóneos para la bioadhesión eran los polímeros más
“empapables”: los dotados de la mayor concentración
de grupos carboxilo, que si bien se adherían a la mucosa intestinal,
penetraban escasamente y liberaban las proteínas con excesiva rapidez.
Mathiowitz estudió los polianhídridos, polímeros
bioadhesivos hidrófobos, que repelen el agua y presentan grupos
carboxilos en el exterior cuando se erosiona su superficie externa. En
1997 observó que se unían a la mucosa intestinal tan bien
como los polímeros hidrofílicos y que, tras cruzar la mucosa
intestinal, alcanzaban la corriente sanguínea de forma más
rápida. Un polianhídrido en particular, el polifumárico-sebácico-anhídrido,
demostró poseer fuerzas adhesivas máximas. Actualmente,
se está utilizando este principio para desarrollar un tipo de insulina
que se pueda administrar por vía oral. La razón por la que
muchos de los nuevos procedimientos de administración se ensayan
con insulina es porque los diabéticos deben inyectarse esta proteína
varias veces al día. En los ensayos con animales, el polianhídrido
dio resultados prometedores, lo mismo con proteínas hidrófilas
que hidrófobas.
Peppas y sus colaboradores también han desarrollado polímeros
bioadhesivos que se hinchan en respuesta a cambios de pH. Podrían
proteger a la insulina del pH ácido del estómago y liberarla
en el pH más alcalino del intestino. Los polímeros también
pueden brindar protección frente a las proteasas del intestino
proximal y abrir temporalmente las uniones entre las células intestinales
permitiendo que el fármaco penetre por los intersticios.
Otra estrategia para la administración oral de fármacos
proteínicos consiste en asociarlos a moléculas que las transporten
a través de la mucosa. En Emisphere Technologies de Tarrytown,
Nueva York, se han desarrollado transportadores moleculares que modifican
las proteínas y reducen su tamaño para que puedan cruzar
mejor las membranas celulares. Una vez desempeñado su cometido
(introducir el fármaco en el interior celular), la molécula
transportadora se rompe y la proteína vuelve a su forma activa
nativa.
Emisphere está ensayando el método con insulina para diabéticos
y también con heparina, una proteína anticoagulante que
reciben las personas a las que se les va a colocar una prótesis
de cadera y que, en ocasiones, desarrollan coágulos sanguíneos.
Otros científicos trabajan en unir fármacos proteínicos
a moléculas con receptores específicos en el tracto gastrointestinal.
Gregory J. Russell-Johnes de Biotech Australia en Roseville, Nueva Gales
del Sur, ha sacado provecho de los receptores de las células intestinales
que fijan la vitamina B12 y la transportan a través de la pared
intestinal. Descubrió que si unía una proteína a
la vitamina B12, los receptores introducían en la célula
tanto la proteína como la misma vitamina. Desafortunadamente, el
número de receptores de vitamina B12 pudiera no bastar para conseguir
que una cantidad suficiente de fármaco alcanzara la sangre y tuviera
un efecto terapéutico. Otros investigadores están realizando
ensayos parecidos con lectinas, unas moléculas muy adhesivas y
mucho más abundantes. Son propias del tejido conjuntivo que hay
entre las células intestinales.
A través de la piel
El intestino es una vía de acceso muy directa a la corriente sanguínea,
pero la piel resulta mucho más accesible. Si bien la piel puede
ser una barrera bastante impermeable, algunos fármacos presentan
características físicas y químicas que les permiten
alcanzar el torrente circulatorio en cantidad suficiente.
Quién no conoce los parches transdérmicos, que duran hasta
siete días y con distintas aplicaciones: de nicotina para dejar
de fumar, o de estradiol, un estrógeno, para combatir los síntomas
de la menopausia o como método anticonceptivo.
Mediante iontoforesis, esto es, la aplicación directa sobre la
piel de una pequeña corriente eléctrica, se puede permeabilizar
la epidermis a muchos fármacos, proteínas incluidas. Se
precisan dos parches con carga eléctrica opuesta, positiva el uno
y negativa el otro, conectados a un reservorio de medicación. Un
pulso de electricidad, indoloro, impulsa al fármaco, habitualmente
dotado de carga eléctrica, a través de la capa externa de
la epidermis hasta los vasos sanguíneos de la dermis.
Vyteris, filial de Becton Dickinson en Fair Lawn, New Jersey, ha solicitado
el permiso de la FDA para comercializar un sistema de iontoforesis para
lidocaína, un analgésico.
(Ver imagen 2)
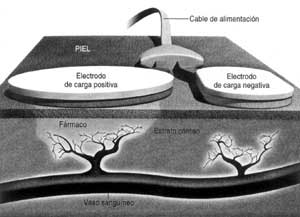
A traves de la piel
RETOS: el resistente estrato córneo (la capa más
externa de la piel) bloquea la entrada de fármacos; muchas moléculas
tienen dificultad para cruzar la epidermis y alcanzar los vasos sanguíneos
de la dermis.
SOLUCIONES: la iontoforesis (abajo) utiliza pulsos de
electricidad indoloros para conseguir la permeabilidad de la piel; los
ultrasonidos emplean ondas sonoras que abren de forma transitoria microcanales
en la capa externa de la epidermis.
La pila es tan pequeña, que se puede llevar debajo de la ropa.
La empresa considera el desarrollo de ensayos clínicos para valorar
la administración de dosis diaria de hormona paratiroidea en pacientes
con osteoporosis o de pulsos de hormona liberadora de gonadotropinas cada
90 minutos en mujeres que se preparan para una fertilización in
vitro.
|