Aspectos Instrumentales
de la Calidad Analítica
Ocho años de historia y nuevos requerimientos
El desempeño inadecuado de los instrumentos en el laboratorio
clínico es una de las causas que con mayor frecuencia produce errores
en el laboratorio clínico y su control es una tarea inherente e
indelegable del profesional a cargo del mismo.
Errores Volumétricos, Termométricos
y Fotométricos
La determinación de parámetros enzimáticos en el
laboratorio de Química Clínica requiere del mayor cuidado
por parte del bioquímico ya que a la falta de estándares
de comparación hay que sumar el cuidadoso mantenimiento de las
condiciones de reacción ( Temperatura, Relación de concentraciones,
estabilidad de reactivos preparados, etc.) Cuando determinamos una enzima
en el laboratorio utilizando un método cinético comercial,
con uso de factores de cálculo de resultados pre-calibrados, si
cometemos un error en el volumen de muestra y/o reactivo, arrastramos
indudablemente ese error al resultado final del paciente. Por ejemplo
si la técnica para la valoración de la enzima Fosfatasa
Alcalina indica que se debe agregar 20 microlitros de suero y la micropipeta
que utilizamos tiene un volumen de 17 microlitros, directamente trasladamos
un error del 15 % al resultado de la misma.. También debemos tener
en cuenta la temperatura de reacción. En el ejemplo anterior, si
la reacción se lleva a cabo a 35º C en lugar de los 37º
C utilizados por el fabricante introducimos un error aproximado del 14
% en el resultado del paciente (se calcula un incremento en la actividad
enzimática del orden del 7% por cada grado de aumento de temperatura).
Si además cometemos un error fotométrico en la lectura eso
hará que, por más que utilicemos una marca de reactivos
de primera calidad, serán inevitables los errores en la fase analítica.
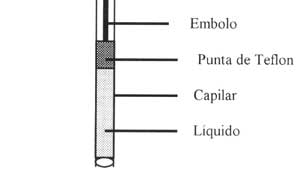
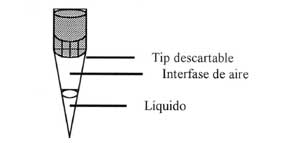
Requerimientos de Calidad Instrumental
Espectrofotómetros, Fotocolorímetros, Autoanalizadores,
Balanzas, Centrífugas, Lectores de Placas, Coagulómetros,
Fotómetros de llama, Instrumental de vidrio, Pipetas y Micropipetas,
Dispensadores, dilutores, Termómetros, Baños de agua , Estufas,
Cubetas Termostatizadas, Heladeras, Freezers, etc., necesitan de controles
de calidad para verificar su buen funcionamiento. En el laboratorio Clínico
debe existir un Programa de control de calidad Interno donde se deben
establecer protocolos de verificación que incluyan los Procedimientos,
las frecuencias de los controles, Registros de dichos controles, Estándares
a cumplir y acciones correctivas si fueran necesarias. Estos procedimientos
de control deben ser llevados a cabo por personal especializado del laboratorio
y no debe confundirse con el Servicio Técnico cuya función
es la de reparar y acondicionar el instrumental de laboratorio. El Programa
de Control de Calidad Instrumental Interno debe verificar el buen desempeño
del mismo.
Los autoanalizadotes deben controlarse?
Esta pregunta muchas veces se hace sin reparar en el hecho que la diferencia
entre estos equipos y las técnicas manuales, es que se automatizan
varias etapas del procedimiento analítico como ser el dispensado
de reactivos y muestras, mezclado, incubación, lectura y cálculo
de resultados, pero tienen en común un fotocolorímetro de
filtros interferenciales el cual debe controlarse de la misma forma que
los manuales. Es más, a pesar de demostrarse a través del
PEEC instrumental que se desempeñan mejor que los Espectrofotómetros
manuales, cerca del 25 % de los mismos presentaron comportamientos no
aceptables cuando se les midió la linealidad fotométrica.
Esta propiedad fotométrica es fundamental pues si el equipo automático
no presenta linealidad aceptable y se calibra el autoanalizador con un
solo calibrador a un nivel dado de concentración, se pueden cometer
grandes errores en las determinaciones analíticas sobre todo en
los niveles de concentración no abarcados en la calibración.
Creación del Programa de Control Instrumental del PEEC
Cuando en el Programa Externo de Evaluación de la Calidad (PEEC)
de la Fundación Bioquímica Argentina se analizaron las causas
de producción de errores mas frecuentes en Química Clínica
se coincidió en que la falta de control del Instrumental era un
factor primordial a revertir.
Esto nos llevó, a principios de 1995 a implementar un programa
de Control de Calidad Instrumental cuyos objetivos fueron que el propio
profesional verificara el buen desempeño del instrumental de laboratorio
para minimizar la producción de errores analíticos y acompañar
al programa de Control de Calidad Interno de Química Clínica
para la toma de decisiones. El esquema básico de cada encuesta
del Programa consistió en el envío a cada uno de los participantes
de información previa, instructivos y los materiales necesarios
para la verificación del instrumento analizado. En el caso de los
espectrofotómetros, colorímetros y autoanalizadores se describió
cada propiedad espectrofotométrica y se remitieron las soluciones
de referencia correspondientes .Los participantes efectuaron los controles
y enviaron los resultados obtenidos. El PEEC analizó los datos
de todos los laboratorios, mandando a cada uno las conclusiones generales
y el desempeño de su aparato de medida.
Encuestas del PEEC instrumental
El cronograma de entrega de materiales de control es cuatrimestral. Hasta
la fecha se han enviado 27 encuestas, incluyendo controles fotométricos
y volumétricos
Para controlar la Exactitud de la Longitud de Onda se eligió el
método del Punto Isosbéstico para que los laboratorios realizaran
los barridos espectrofotométricos de las soluciones ácida
y alcalina de distintos colorantes (Rojo
Congo, Azul de Bromotimol) y determinaran el corrimiento en la longitud
de onda de su espectrofotómetro.
Para el control de la Exactitud Fotométrica se utilizaron soluciones
de Dicromato de Potasio en medio perclórico para controlar la zona
del UV, soluciones de Nitrato de Cobalto para el visible (510 nm) y cianmetahemoglobina
para los 540 nm.
Para comprobar la Linealidad Fotométrica se enviaron 4 soluciones
de Dicromato de Potasio de distinta concentración para el control
a 340 nm, 4 soluciones de p-nitrofenol en medio alcalino para controlar
la zona de 405 nm, y 4 soluciones de nitrato de Cobalto para los 510 nm.
Para detectar la Luz Parásita se envió a los laboratorios
una solución de Nitrito de sodio.
También en otras encuestas se evaluó la Precisión
Fotométrica enviando a todos los participantes una solución
de sulfato cúprico en medio ácido.
Asimismo se evaluó la Estabilidad Fotométrica enviando una
solución de Dicromato de Potasio con el fin de detectar la presencia
de Deriva y Ruido fotométrico.
Como control volumétrico de micropipetas se evaluó la exactitud
del volumen dispensado mediante el método fotométrico utilizando
un lisado de hemoglobina y reactivo de Drabkin.
Preparación de los Materiales de Control: LARESBIC
La preparación de las soluciones y las mediciones para su certificación
se realizan en el Laboratorio de Referencia y Estandarización en
Bioquímica Clínica (LARESBIC) de la Fundación Bioquímica
Argentina. Este Laboratorio de Referencia cuenta con Materiales de Referencia
Certificados por el NIST para todas las propiedades fotométricas
que se evalúan en las encuestas:
• SRM 935 a: Dicromato de Potasio Cristalino para ser usado como
estándar de Absorbancia en el UV
• SRM 931 f: Estándares Líquidos de Absorbancia para
espectrofotometría UV y Visible
• SRM 2032: Ioduro de Potasio Cristalino para ser usado como estándar
en la detección de luz parásita en el UV.
• SRM 2034: Solución de Oxido de Holmio: estándar
de Longitud de Onda entre 240 nm y 650 nm.
LARESBIC cuenta con un espectrofotómetro con arreglo de diodos
Hewlett-Packard 8453, cuyo funcionamiento es controlado mediante el uso
de los estándares de referencia antes listados. Las soluciones
para las encuestas son preparadas siguiendo los procedimientos detallados
en el estándar ASTM E - 925 – 83 y las medidas de absorbancia
para la certificación se realizan en el espectrofotómetro
Hewlett-Packard 8453, transfiriendo de esta manera la trazabilidad a los
estándares de referencia del NIST.
A su vez, LARESBIC cuenta con materiales de referencia para la medición
de temperaturas en el rango clínico. Como material de referencia
primario posee una celda de Galio (SRM 1968- NIST) y como material de
referencia secundario un termómetro de Hg certificado entre 24ºC
y 38ºC (SRM 934- NIST). Ambos instrumentos son utilizados para la
transferencia de trazabilidad a los termómetros, sondas termométricas
y baños termostáticos utilizados de rutina en LARESBIC.
Asimismo se utilizan para la calibración de la sonda termométrica
del espectrofotómetro, de manera de poder medir con exactitud la
temperatura en el interior de la cubeta de reacción. Este paso
es fundamental para la medición de absorbancias de soluciones cuyo
coeficiente de extinción cambia con la temperatura.
Por último, LARESBIC cuenta con un juego de pesas certificadas
clase E2 en el rango de 0.5 g a 200 g. Dichas pesas se utilizan en la
calibración de la balanza con la cual se pesan las drogas necesarias
para la preparación de las soluciones y se realizan los controles
de pipetas de doble aforo y micropipetas por el método gravimétrico.
Kit de Control Instrumental Interno
Desde hace un año los laboratorios cuentan con un servicio adicional.
Se instrumentó desde el Programa la provisión de material
de control fotométrico acondicionado para que el bioquímico
pueda fácilmente controlar su equipo de lectura fotométrico,
sea manual o automático. Incluye ampollas de soluciones certificadas
para controlar EXACTITUD FOTOMÉTRICA, PRECISIÓN FOTOMÉTRICA,
EXACTITUD DE LA LONGITUD DE ONDA, LINEALIDAD FOTOMÉTRICA, LUZ PARÁSITA,
DERIVA Y RUIDO FOTOMÉTRICO. Su costo es de 72 $ y está diseñado
para permitir el control anual de 1 espectrofotómetro.
Calibración de Pipetas para los participantes del PEEC
Sabido es la dificultad que tenemos los laboratorios de proveernos de
material volumétrico clase A o B debidamente certificado y teniendo
en cuenta la importancia que tiene disolver un calibrador o un suero control
con el correcto volumen de agua, desde el programa se adquirieron pipetas
de 1,3 y 5 ml de doble aforo, se las recalibró por el método
gravimétrico y se las envió a los participantes del PEEC
en un envase especial. Es de destacar que fue preciso descartar el 32.5
% de las pipetas de 1 ml ya que no cumplían con la tolerancia exigida.
(Ver tabla)
Volumen
nominal |
Tolerancia
(clase B) |
Nº |
% fuera
de rango |
5 ml |
+/- 20 ul
(4.98 -5.02 ul) |
820 |
2.7 % |
3 ml |
+/- 20 ul
(2.98 – 3.02 ul) |
400 |
1.8 % |
1 ml |
+/- 20 ul
(0.98 – 1.02 ul) |
100 |
32.5 % |
Plantel Profesional
El programa es dirigido por el Dr. Claudio Duymovich y las Dras Rosana
Acheme y Sandra Sesini siendo supervisado por el Dr. Daniel Mazziotta,
Director del Programa de Evaluación Externa de la Fundación
Bioquímica Argentina.
|